题目内容
3.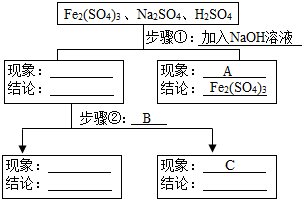 某同学设计鉴别物质引导图图下:
某同学设计鉴别物质引导图图下:回答下列问题:
(1)A为产生红褐色沉淀,此反应的化学方程式为Fe2(SO4)3+6NaOH=2Fe(OH)3↓+3Na2SO4.
(2)B为滴加紫色石蕊试剂(滴加Na2CO3溶液)(合理即可).
(3)C为溶液显红色(或有气泡产生等)(合理即可).
分析 根据硫酸铁能与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀,硫酸能与氢氧化钠溶液生成硫酸钠和水,但无明显变化;硫酸钠不能与氢氧化钠溶液反应;据此结合酸的化学性质,进行分析解答.
解答 解:(1)硫酸铁能与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀,硫酸能与氢氧化钠溶液生成硫酸钠和水,但无明显变化;硫酸钠不能与氢氧化钠溶液反应;故A为产生红褐色沉淀;反应的化学方程式为:Fe2(SO4)3+6NaOH=2Fe(OH)3↓+3Na2SO4.
(2)剩余的两种溶液为硫酸钠、硫酸溶液,硫酸能显酸性,能使紫色石蕊试液(或碳酸钠溶液等)变红色(或产生气泡等),硫酸钠不能使紫色石蕊试液变色.
(3)能使紫色石蕊试液变红色的是硫酸,不变色的是硫酸钠溶液.
故答案为:(1)产生红褐色沉淀;Fe2(SO4)3+6NaOH=2Fe(OH)3↓+3Na2SO4;
(2)滴加紫色石蕊试液(滴加Na2CO3溶液)(合理即可);
(3)溶液显红色(或有气泡产生等)(合理即可).
点评 本题有一定难度,解答物质的鉴别题时要熟练掌握鉴别的物质的性质,然后选择适当的试剂或方法,出现不同的现象即可鉴别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.已知在相同的温度和压强下,任何气体的体积与分子数成正比,N2中可能混有HCl、CO2、CO、H2四种气体中的一种或几种,把气体依次通过饱和碳酸氢钠溶液、足量氢氧化钠溶液、灼热的氧化铜,气体体积变化依次为:不变、变小、变小.则下列判断正确的是( )
| A. | 一定混有HCl | B. | 一定混有CO | C. | 一定混有CO2 | D. | 一定混有H2 |
18.某物质不含碳元素和氢元素,则该物质不可能是( )
①酸 ②碱 ③盐 ④有机物.
①酸 ②碱 ③盐 ④有机物.
| A. | ①②④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
8.下列属于不可再生能源的是( )
| A. | 煤 | B. | 太阳能 | C. | 风能 | D. | 氢能 |
13.下列属于纯净物的是( )
| A. | 糖水 | B. | 金刚石 | C. | 空气 | D. | 石油 |
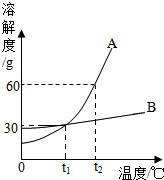 如图是A、B两种物质的溶解度曲线,请回答:
如图是A、B两种物质的溶解度曲线,请回答:
 用科学方法认识和改造物质
用科学方法认识和改造物质