题目内容
5.化学实验是学习化学的基础,请根据如图所示回答问题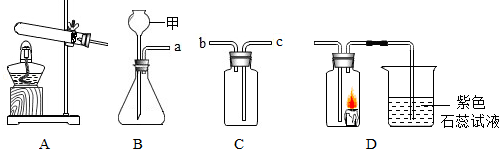
(1)仪器甲的名称是长颈漏斗
(2)实验室用高锰酸钾制取氧气,选择A做发生装置时,试管口应放一团棉花,棉花的作用是防止高锰酸钾粉末进入导管
(3)若装置C中装半瓶浓硫酸,连接装置B、C、D,可以同时景象实验室制取气体和物质性质的验证实验.
①若实验时D中蜡烛熄灭,紫色石蕊溶液变红,则B中反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若实验时D中蜡烛燃烧的更旺,紫色石蕊溶液变红则B中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③C中浓硫酸的作用是吸收水分,起干燥作用,B中的导管口a应与C中的导管口c(填“b”或“c”)连接.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.若实验时D中蜡烛燃烧的更旺,紫色石蕊溶液变红是因为:产生氧气使蜡烛燃烧更旺;蜡烛燃烧产生的CO2与石蕊溶液中的水反应,生成碳酸;那么B中生成的是氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平.浓硫酸的作用是:吸收水分,起干燥作用;B中的导管口a应与C中的导管口c相连,因为二氧化碳和氧气的密度都比空气的密度大.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗
(2)加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;故答案为:防止高锰酸钾粉末进入导管;
(3)①碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可,故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑
②若实验时D中蜡烛燃烧的更旺,紫色石蕊溶液变红是因为:产生氧气使蜡烛燃烧更旺;蜡烛燃烧产生的CO2与石蕊溶液中的水反应,生成碳酸;那么B中生成的是氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③浓硫酸的作用是:吸收水分,起干燥作用;B中的导管口a应与C中的导管口c相连,因为二氧化碳和氧气的密度都比空气的密度大;故答案为:吸收水分,起干燥作用(或做干燥剂);c;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 小题狂做系列答案
小题狂做系列答案| A. | 金属锈蚀 | B. | 冰雪融化 | C. | 煤气燃烧 | D. | 燃放鞭炮 |
| A. | 氧气 | B. | 蒸馏水 | C. | 洁净的空气 | D. | 氮气 |
| A. | 由CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2可知,CO具有还原性 | |
| B. | 金刚石、石墨、C60完全燃烧都生成CO2 | |
| C. | CO2能使干燥的紫色石蕊纸花变红 | |
| D. | CO有毒,CO2无毒 |
| A. | 20% | B. | 15% | C. | 10% | D. | 25% |
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | B. | 6HCl+2Fe=2FeCl3+3H2↑ | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | 2KClO3=2KCl+3O2↑ |
| A. | 干冰用于人工降雨 | B. | 氧气用于气焊 | ||
| C. | 盐酸用于除铁锈 | D. | 小苏打用于治疗胃酸过多 |
| A. | 从铝土矿(主要成分是Al2O3)中提炼金属铝 | |
| B. | 秸秆、杂草、粪便等在沼气池中发酵 | |
| C. | 二氧化碳气体经加压、降温得到干冰 | |
| D. | 一氧化碳燃烧生成二氧化碳 |
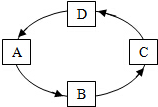 已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.
已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.