题目内容
5.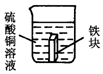 如图所示,一杯硫酸铜溶液,液体对杯底产生的压强为p1,在这杯溶液中浸入一铁块,此时液体对杯底的压强为p2;铁块放一段时间后取出(水分质量不损失),这时液体对杯底的压强为p3.
如图所示,一杯硫酸铜溶液,液体对杯底产生的压强为p1,在这杯溶液中浸入一铁块,此时液体对杯底的压强为p2;铁块放一段时间后取出(水分质量不损失),这时液体对杯底的压强为p3.(1)p1、p2、p3,由小到大的顺序是p3、p1、p2;
(2)其中发生反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.
分析 根据液体压强公式p=ρgh,以及反应前后的溶液质量变化分析.
解答 解:因为液体压强公式p=ρgh,在这杯溶液中浸入一铁块,液体的液面上升,液体的高度(h)变大,所以此时液体对杯底的压强变大,所以p1<p2;铁块放后铁与硫酸铜反应生成氯化亚铁和铜,
即Fe+CuSO4=FeSO4+Cu
56 64
可知每56份质量的铁置换64份质量的铜,所以随着反应的进行溶液的质量减小,溶液的体积基本不变,所以溶液的密度增加,根据液体压强公式p=ρgh,所以p3<p1;所以p1、p2、p3,由小到大的顺序是:p3、p1、p2.
故答案为:(1)p3、p1、p2;(2)Fe+CuSO4=FeSO4+Cu.
点评 本题考查了压强定义式、密度公式、化学方程式的掌握和运用,在明确容器中的液体密度关系后,通过分析排开液体的体积对h造成的影响是本题的关键所在.

练习册系列答案
相关题目
15.下列气体中可用NaOH做干燥剂的是( )
| A. | CO2 | B. | HCl | C. | H2 | D. | SO2 |
16.下列实验操作错误的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
13.洗衣机减轻了人们的劳动强度,下列说法中正确的是( )
| A. | 洗涤剂加水稀释后溶质质量分数变大 | |
| B. | 洗涤后衣服上一定没有残留洗涤液 | |
| C. | 洗涤后排除的液体一定是溶液 | |
| D. | 洗涤时适当提高水温能加快洗衣粉溶解 |
20.由N、O两种元素组成的化合物中N、O的质量比为7:16则该化合物化学式为( )
| A. | NO | B. | N2O | C. | NO2 | D. | N2O6 |
10.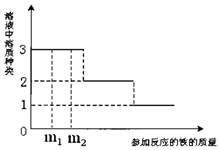 某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的铁粉进行处理,并绘制参加反应的铁与溶液中溶质种类的关系图.下列说法正确的是( )
某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的铁粉进行处理,并绘制参加反应的铁与溶液中溶质种类的关系图.下列说法正确的是( )
 某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的铁粉进行处理,并绘制参加反应的铁与溶液中溶质种类的关系图.下列说法正确的是( )
某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的铁粉进行处理,并绘制参加反应的铁与溶液中溶质种类的关系图.下列说法正确的是( )| A. | 当溶质种类为2种时,金属单质种类可能为2种 | |
| B. | 当参加反应的铁的质量为m1时,溶质的种类、金属单质种类均为3种 | |
| C. | 当参加反应的铁的质量为m1、m2时,两者溶液中Cu(NO3)2质量分数相等 | |
| D. | 当溶质种类为1种时,金属单质种类可能为1种 |
15.蜡烛燃烧的过程中( )
| A. | 只发生物理变化 | B. | 只发生化学变化 | ||
| C. | 没有发生物理变化 | D. | 既有物理变化又有化学变化 |