题目内容
9.四个烧杯中分别盛有饱和澄清石灰水、稀盐酸、氯化钠溶液、碳酸钠溶液中的一种.向其中分别滴加无色酚酞溶液或紫色石蕊溶液(如图所示).选用下列药品继续实验:铁粉、氧化钙、氧化铁、稀盐酸、饱和澄清石灰水、碳酸钠溶液,请依据实验回答问题.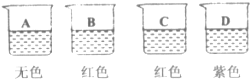
(1)D是氯化钠溶液.
(2)取A中溶液于试管中,加入甲,溶液由无色变为黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
(3)取B中溶液于试管中,加入乙,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,无气泡产生,则乙的化学式为Ca0.
(4)取c中溶液于试管中,加入丁,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,同时产生气泡.
①用化学方程式表示溶液变浑浊的原因:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.②最终所得溶液中溶质的组成为CaCl2、HCl、NaCl或CaCl2、NaCl(写出所有可能).
【拓展】小明取少量氢氧化钠溶液于试管中,加入丙,未观察到明显的现象.小刚改进了实验:取少量氢氧化钠溶液于试管中,先向其中加入铁粉,无明显现象,再逐滴加入丙.开始时没有气泡,持续滴加后产生气泡,说明氢氧化钠溶液与丙发生了反应.
请你再设计一个实验(写出实验操作及现象),也能证明氢氧化钠溶液与丙发生了反应.
取氢氧化钠溶液于试管中,先向其中滴加适量的酚酞溶液,再逐滴加入丙溶液,溶液由红色变为无色,说明氢氧化钠溶液与丙发生了反应
【反思】在我们已经学过的化学反应中,有些反应伴随着明显的状态变化等现象,有些反应没有明显的现象出现,我们可以通过借助其它试剂或改变实验装置将无现象实验显性化,从而获得结论.
分析 (1)石灰水和碳酸钠溶液显碱性,能使酚酞试液变红色,能使石蕊试液变蓝色,稀盐酸显酸性,能使石蕊试液变红色,不能使酚酞试液变色,氯化钠溶液显中性,变色石蕊试液、酚酞试液变色;
(2)氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色溶液;
(3)饱和石灰水中加入氧化钙时,氧化钙和水反应生成氢氧化钙,同时放热,温度升高,氢氧化钙溶解度减小,部分氢氧化钙析出,氢氧化钙和稀盐酸反应生成氯化钙和水;
(4)碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
【拓展】
氢氧化钠和稀盐酸反应生成氯化钠和水,氢氧化钠溶液显碱性,能使酚酞试液变红色.
解答 解:(1)D溶液显紫色,说明D溶液是氯化钠溶液.
故填:氯化钠.
(2)取A中溶液于试管中,加入甲,溶液由无色变为黄色,则A是稀盐酸,甲是氧化铁,稀盐酸和氧化铁反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
故填:Fe2O3+6HCl═2FeCl3+3H2O.
(3)根据浑浊的溶液中加入丙无气泡产生,说明浑浊的原因不是产生了碳酸盐沉淀,由于氧化钙能与水反应生成氢氧化钙,而使饱和的石灰水变浑浊,可知B中盛有的是饱和石灰水,加入的乙是氧化钙.
故填:CaO.
(4)(4)根据浑浊的溶液中加入丙有气泡产生,说明浑浊的原因是产生了碳酸盐沉淀,则C中盛有的是碳酸钠溶液,加入的是氢氧化钙溶液,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
加入盐酸,由于溶液变为无色,无色溶液可能呈中性,也可能成酸性,故溶质可能是氯化钠、氯化钙,也可能是氯化钠、氯化钙、氯化氢.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;CaCl2、HCl、NaCl或CaCl2、NaCl.
【拓展】
证明氢氧化钠溶液与丙发生了反应的实验方案为:取氢氧化钠溶液于试管中,先向其中滴加适量的酚酞溶液,再逐滴加入丙溶液,溶液由红色变为无色,说明氢氧化钠溶液与丙发生了反应.
故填:取氢氧化钠溶液于试管中,先向其中滴加适量的酚酞溶液,再逐滴加入丙溶液,溶液由红色变为无色,说明氢氧化钠溶液与丙发生了反应.
【反思】
在我们已经学过的化学反应中,有些反应伴随着明显的状态变化等现象,有些反应没有明显的现象出现,我们可以通过借助其它试剂或改变实验装置将无现象实验显性化,从而获得结论.
故填:借助其它试剂或改变实验装置.
点评 本题考查了常见物质成分的推断,完成此题,可以依据物质的性质进行.要注意根据反应的实验现象进行判断.

| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2气体 | SO2 | 通入石灰水 |
| B | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| C | 炭粉 | CuO粉末 | 加入过量稀硫酸,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 某品牌纯净水 | B. | 清新的空气 | C. | 石灰水 | D. | 蒸馏水 |
| A. | 用一氧化碳冶炼金属:CO+O2$\frac{\underline{\;燃烧\;}}{\;}$CO2 | |
| B. | 用适量盐酸清除铁锈:Fe2O3+6HCl═2FeCl2+3H2O | |
| C. | 用红磷燃烧测定空气中氧气的含量:4P+5O2↑$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | |
| D. | 高温燃烧石灰石制取生石灰:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
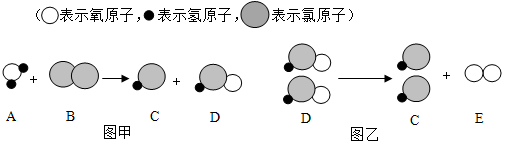
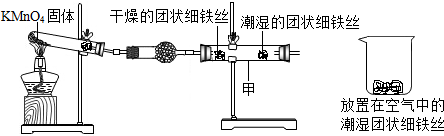
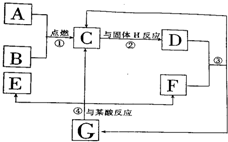 初中化学中几种常见物质有如图所示的转化关系,其中A、B常温下为气体单质,反应④常用于实验室制F气体,G为难溶于水的白色固体.
初中化学中几种常见物质有如图所示的转化关系,其中A、B常温下为气体单质,反应④常用于实验室制F气体,G为难溶于水的白色固体.