题目内容
13.现有一包固体粉末,可能是K2CO3、K2SO4、CuSO4、KCl中的一种或几种,为了测定其组成,取适量样品进行下列实验,(1)取样品溶于水,得到无色澄清溶液;
(2)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀.过滤,向沉淀中加入过量的稀硝酸,沉淀部分消失并产生气泡;
(3)取步骤(2)试验后的滤液,加入稀硝酸化后,再加入AgNO3溶液,出现白色沉淀.A、B、C、D四位同学根据实验现象分别判断出此固体粉末中一定含有的物质,判断正确同学是( )
| A. | K2CO3、CuSO4 | B. | K2CO3、KCl | C. | K2CO3、K2SO4 | D. | K2CO3、K2SO4、KCl |
分析 根据硫酸铜在溶液中显蓝色,硫酸钾和氯化钡会生成不溶于酸的硫酸钡沉淀,碳酸钾和氯化钡会生成溶于酸的碳酸钡沉淀,氯离子和硝酸银会生成氯化银沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,硫酸钾和氯化钡会生成不溶于酸的硫酸钡沉淀,碳酸钾和氯化钡会生成溶于酸的碳酸钡沉淀,氯离子和硝酸银会生成氯化银沉淀.
取样品溶于水,得到无色澄清溶液,硫酸铜在溶液中显蓝色,所以固体粉末中一定不含硫酸铜;取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀.过滤,向沉淀中加入过量的稀硝酸,沉淀部分消失并产生气泡,所以固体粉末中一定含有硫酸钾、碳酸钾;取步骤(2)试验后的滤液,加入稀硝酸化后,再加入AgNO3溶液,出现白色沉淀,氯化钡引入了氯离子,所以不能判断粉末中是否含有氯化钾,所以固体粉末中一定含有硫酸钾、碳酸钾.
故选:C.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
4.下列物质长期暴露在空气中,因发生化学变化而使溶液质量减小的是( )
| A. | 氯化钠溶液 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 氢氧化钙溶液 |
8. 水是生命之源.“生命吸管”是一项简单却有意义的发明,新一代“生命吸管”是在塑料管中装有活性炭符合滤芯和0.01微米超滤物理过滤,过滤掉水中杂质和有害病菌,把河水等过滤消毒成可饮用水;该装置能为飓风、地震或其它灾难的受害者提供安全的饮用水,还可以成为人们周末外出旅游随身携带的“武器”.下列有关水的说法正确的是( )
水是生命之源.“生命吸管”是一项简单却有意义的发明,新一代“生命吸管”是在塑料管中装有活性炭符合滤芯和0.01微米超滤物理过滤,过滤掉水中杂质和有害病菌,把河水等过滤消毒成可饮用水;该装置能为飓风、地震或其它灾难的受害者提供安全的饮用水,还可以成为人们周末外出旅游随身携带的“武器”.下列有关水的说法正确的是( )
 水是生命之源.“生命吸管”是一项简单却有意义的发明,新一代“生命吸管”是在塑料管中装有活性炭符合滤芯和0.01微米超滤物理过滤,过滤掉水中杂质和有害病菌,把河水等过滤消毒成可饮用水;该装置能为飓风、地震或其它灾难的受害者提供安全的饮用水,还可以成为人们周末外出旅游随身携带的“武器”.下列有关水的说法正确的是( )
水是生命之源.“生命吸管”是一项简单却有意义的发明,新一代“生命吸管”是在塑料管中装有活性炭符合滤芯和0.01微米超滤物理过滤,过滤掉水中杂质和有害病菌,把河水等过滤消毒成可饮用水;该装置能为飓风、地震或其它灾难的受害者提供安全的饮用水,还可以成为人们周末外出旅游随身携带的“武器”.下列有关水的说法正确的是( )| A. | 河水、湖水是混合物,通过“生命吸管”可变为纯水 | |
| B. | “生命吸管”可把硬水变为软水 | |
| C. | 把水煮沸,水分子的运动速率和间隔都增大 | |
| D. | 电解水生成氢气和氧气,说明水是由氢气和氧气组成的 |
5.分类学习是化学重要的学习思想,下列物质分类错误的一组是( )
| A. | He、O3、C | B. | H2CO3、H2SO4、HNO3 | ||
| C. | KOH、Ca(OH)2、C2H5OH | D. | AlCl3、Na2CO3、NH4Cl |
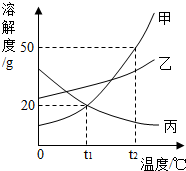 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息回答下列问题:
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息回答下列问题: