题目内容
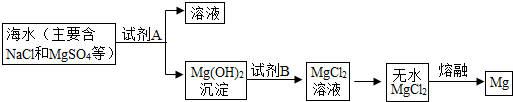
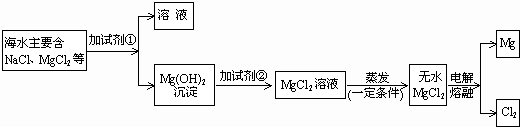
镁是一种用途很广泛的金属材料,目前世界上60%的镁是从海水中提取的.其主要溶 液试剂A试剂BMgCl2溶液无水MgCl2MgMg(OH)2沉淀海水(主要含NaCl和MgSO4等)步骤如下图:

(1)提取Mg的过程中,试剂A可以选用
(2)分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的氯钡溶液、碳酸钠溶液,过滤后再向滤液中加入适量盐酸.则加入氯化钡溶液后的反应方程式为
加入过量碳酸钠溶液的目的是除去

(1)提取Mg的过程中,试剂A可以选用
氢氧化钠
氢氧化钠
,试剂B选用稀盐酸
稀盐酸
;(2)分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的氯钡溶液、碳酸钠溶液,过滤后再向滤液中加入适量盐酸.则加入氯化钡溶液后的反应方程式为
BaCl2+Na2SO4═2NaCl+BaSO4↓
BaCl2+Na2SO4═2NaCl+BaSO4↓
;加入过量碳酸钠溶液的目的是除去
Ba2+、Ca2+
Ba2+、Ca2+
(填离子符号).分析:(1)根据硫酸镁和氢氧化钠的化学性质回答前一空;根据盐酸和氢氧化镁的化学性质回答后一空.
(2)根据除杂的原则、钙离子和硫酸根离子的性质回答.
(2)根据除杂的原则、钙离子和硫酸根离子的性质回答.
解答:解:(1)要得到氢氧化镁,必须用硫酸镁与可溶性碱反应,常用氢氧化钠,硫酸镁和氢氧化钠反应能生成碳酸钠和氢氧化镁沉淀;要使氢氧化镁转化为氯化镁,必须加入盐酸,盐酸与氢氧化镁发生中和反应,生成氯化镁和水.
(2)要除去氯化钠中的CaCl2、Na2SO4等杂质,实际上是除去钙离子与硫酸根离子,一般采用沉淀法,即把两种离子转化为沉淀后过滤除去,加入氯化钡溶液可除去硫酸根离子,涉及反应方程式为BaCl2+Na2SO4═2NaCl+BaSO4↓;然后再加入过量碳酸钠溶液,让过量的氯化钡与碳酸钠反应生成氯化钠和碳酸钡沉淀,让氯化钙同时与碳酸钠反应生成氯化钠和碳酸钙沉淀,最终除去Ba2+、Ca2+.
故答案为:(1)氢氧化钠;稀盐酸;
(2)BaCl2+Na2SO4═2NaCl+BaSO4↓; Ba2+、Ca2+.
(2)要除去氯化钠中的CaCl2、Na2SO4等杂质,实际上是除去钙离子与硫酸根离子,一般采用沉淀法,即把两种离子转化为沉淀后过滤除去,加入氯化钡溶液可除去硫酸根离子,涉及反应方程式为BaCl2+Na2SO4═2NaCl+BaSO4↓;然后再加入过量碳酸钠溶液,让过量的氯化钡与碳酸钠反应生成氯化钠和碳酸钡沉淀,让氯化钙同时与碳酸钠反应生成氯化钠和碳酸钙沉淀,最终除去Ba2+、Ca2+.
故答案为:(1)氢氧化钠;稀盐酸;
(2)BaCl2+Na2SO4═2NaCl+BaSO4↓; Ba2+、Ca2+.
点评:本题以海水中提取镁为题材,主要考查硫酸镁、氢氧化钠、盐酸、氢氧化镁、氯化钙、硫酸钠等物质的性质,掌握上述物质的化学性质,问题会迎刃而解.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目