题目内容
金属用途广泛,其结构和性质等是化学的重要研究内容.
(1)如图1是铝的原子结构示意图.下列说法不正确的是 .
A.铝原子的质子数为13 B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素 D.铝可作导线是由于它具有良好的导电性
(2)如图2是工业炼铁示意图.其中,焦炭的作用是燃烧提供能量和 ;有铁生成的化学方程式为 .
(3)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁.现有废硫酸49t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少? .

(1)如图1是铝的原子结构示意图.下列说法不正确的是
A.铝原子的质子数为13 B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素 D.铝可作导线是由于它具有良好的导电性
(2)如图2是工业炼铁示意图.其中,焦炭的作用是燃烧提供能量和
(3)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁.现有废硫酸49t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?
考点:铁的冶炼,原子结构示意图与离子结构示意图,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:金属与金属材料
分析:(1)根据铝原子结构示意图和地壳中最多的元素,能做导线的原因考虑本题;
(2)根据焦炭的作用考虑,根据方程式的写法写出反应原理;
(3)根据硫酸质量直接算出硫酸亚铁的质量.
(2)根据焦炭的作用考虑,根据方程式的写法写出反应原理;
(3)根据硫酸质量直接算出硫酸亚铁的质量.
解答:解:(1)原子结构示意图中圆圈内数字就是质子数;所以铝原子质子数是13;由于铝原子最外层电子数是3易失去3个电子,显+3价;地壳中含量最多的元素是氧;铝做导线就是因为铝具有导电性;
(2)因为焦炭燃烧放出大量的热,给炼铁提供热量,同时碳燃烧生成二氧化碳,碳再与二氧化碳反应生成一氧化碳,所以制取一氧化碳,一氧化碳再作为炼铁的还原剂;
(3)设生成硫酸亚铁的质量为x,则:
Fe+H2SO4 ═FeSO4+H2↑
98 152
49t×10% x
=
解得x=7.6t;
答可生产硫酸亚铁的质量是7.6t.
故答案为:(1)C;(2)制取CO;Fe2O3+3CO
2Fe+3CO2;(3)7.6t.
(2)因为焦炭燃烧放出大量的热,给炼铁提供热量,同时碳燃烧生成二氧化碳,碳再与二氧化碳反应生成一氧化碳,所以制取一氧化碳,一氧化碳再作为炼铁的还原剂;
(3)设生成硫酸亚铁的质量为x,则:
Fe+H2SO4 ═FeSO4+H2↑
98 152
49t×10% x
| 98 |
| 49t×10% |
| 152 |
| x |
解得x=7.6t;
答可生产硫酸亚铁的质量是7.6t.
故答案为:(1)C;(2)制取CO;Fe2O3+3CO
| ||
点评:本题考查了原子结构示意图、化学方程式的书写和根据化学方程式的计算,侧重知识的综合应用.

练习册系列答案
相关题目
下列变化不属于缓慢氧化的是( )
| A、铁生锈 | B、呼吸作用 |
| C、蜡烛燃烧 | D、食物腐烂 |
下列物质之中属于纯净物的是( )
| A、矿泉水 | B、液氮 |
| C、澄清石灰水 | D、纯净空气 |
下列各组物质的名称或俗称与化学式不相符的是( )
| A、CaCO3 大理石 碳酸钙 |
| B、NaOH 烧碱 氢氧化钠 |
| C、CaO 生石灰 消石灰 |
| D、Ca(OH)2 熟石灰 氢氧化钙 |
下列实验操作中,不正确的是( )
A、 |
B、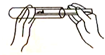 |
C、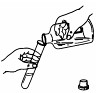 |
D、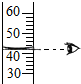 |
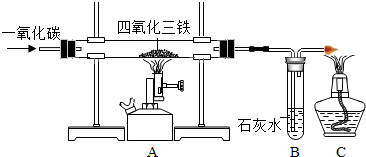 在实验室里,可以利用如图装置制得铁.
在实验室里,可以利用如图装置制得铁.