题目内容
14.下列各组反应(物质均为反应物),反应刚开始时,放出H2的速率最大的是( )| 选项 | 金属(粉末状)/mol | 体积/mL | 酸 | 反应温度/℃ | |
| A | Mg | 0.1 | 10 | HNO3 | 70 |
| B | Mg | 0.1 | 10 | HCl | 70 |
| C | Fe | 0.1 | 10 | HCl | 60 |
| D | Mg | 0.1 | 10 | HNO3 | 60 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据影响反应熟虑的因素分析判断,金属的性质、酸的浓度和反应的温度都会影响反应的速率.
解答 解:金属的活动性是Mg>Fe,硝酸具有强氧化性,不能与金属反应生成氢气,在B中温度高,反应的速率最快.
故选B.
点评 本题的难度不大,了解影响金属与酸反应速率的因素是解答本题的基础知识.

练习册系列答案
相关题目
4. 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
(1)写出试管②中碳酸钠与氢氧化钙反应的化学方式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是可能含有氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理;
因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
【实验分析】小亮同学针对自己的猜想进行了如下实验:
你认为小亮同学对实验结果判断是否正确?请说明理由不正确.因为氢氧化钠存在,滴入几滴稀盐酸量太少,不会立即出现气泡,但碳酸钠可能存在.
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余.
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.(1)写出试管②中碳酸钠与氢氧化钙反应的化学方式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是可能含有氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理;
因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,通入二氧化碳 | 白色沉淀 | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | 自己的猜想不成立 |
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余.
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
2.化学与健康息息相关.“APEC”会议的晚宴上有一道传统小吃“豌豆黄”,根据表格中的信息回答以下问题.
(1)“豌豆黄”中主要含有蛋白质、糖类和无机盐三类营养素.
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起AC(填序号).
A.佝偻病 B.贫血症 C.骨质疏松 D.甲状腺肿大
(3)很多食物也能提供丰富的蛋白质.下列能提供丰富蛋白质的食品是B(填序号).

| 品名 | 豌豆黄 |
| 主要原料 | 豌豆 |
| 主要营养成分 | 蛋白质、糖类、钠、钙、钾、镁、铁等元素 |
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起AC(填序号).
A.佝偻病 B.贫血症 C.骨质疏松 D.甲状腺肿大
(3)很多食物也能提供丰富的蛋白质.下列能提供丰富蛋白质的食品是B(填序号).

2.水是地球上最普通、最常见的物质之一,下列关于水的说法正确的是( )
| A. | 水是所有溶液中的溶剂 | |
| B. | 水电解生成氢气和氧气,说明化学反应中分子可以再分,原子不可再分 | |
| C. | 水的蒸发和水的电解都生成气体,它们都是化学变化 | |
| D. | 水蒸发后,水分子间的间隔增大 |
9.如图所示的化学实验基本操作中,正确的是( )
| A. |  | B. | 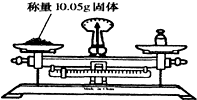 | ||
| C. |  | D. | 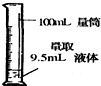 |
 小坤同学发现他家养的鲜花植株矮小,茎秆很细,叶片,发黄,便利用所学知识施加了如图包装袋所示的化肥.计算回答下列问题:
小坤同学发现他家养的鲜花植株矮小,茎秆很细,叶片,发黄,便利用所学知识施加了如图包装袋所示的化肥.计算回答下列问题: 如图是某氯化钠注射液标签的部分内容,取这种NaCl注射液130.0g,滴入足量的AgNO3溶液,充分反应后得到AgCl沉淀2.87g.通过计算判断这种氯化钠注射液中NaCl的质量分数是否和标签相符.
如图是某氯化钠注射液标签的部分内容,取这种NaCl注射液130.0g,滴入足量的AgNO3溶液,充分反应后得到AgCl沉淀2.87g.通过计算判断这种氯化钠注射液中NaCl的质量分数是否和标签相符.