题目内容
19.某混合物中含有碳酸钙和氯化钙,取该混合物12g,向其中加入一定质量的质量分数为10%的稀盐酸,恰好完全反应,产生4.4g气体.(假设气体全部逸出).计算:
(1)所取混合物中碳酸钙的质量.
(2)所加稀盐酸的质量
(3)反应后所得溶液中溶质的质量分数(计算结果精确到0.1%)
分析 根据生成二氧化碳的质量可以求出碳酸钙、氯化氢、氯化钙的质量,从而可以计算石灰石中碳酸钙的质量分数、生成的氯化钙的质量、稀盐酸中溶质的质量,再根据反应后溶质的质量分数求出反应后的溶液中的质量分数以及反应前稀盐酸的质量
解答 解:(1)设碳酸钙、氯化氢、氯化钙的质量分别为x、y、z,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 111 44
x y z 4.4g
$\frac{100}{x}=\frac{73}{y}=\frac{111}{z}=\frac{44}{4.4g}$
x=10g,y=7.3g,z=11.1g,
(2)所加稀盐酸的质量=$\frac{7.3g}{10%}$=73g;
(3)反应后溶液中的氯化钙包括反应生成的和混合物中本来就有的,其质量=11.1g+12g-10g=13.1g,反应后所得溶液中的质量分数=$\frac{13.1g}{12g+73g-4.4g}$=16.3%
故答案为:
(1)石灰石中碳酸钙的质量为10g;
(2)反应前稀盐酸的质量为73g;
(3)反应后所得溶液中的质量分数为16.3%
点评 本题难度较大,主要考查了以化学方程式计算为基础,同时融入溶液等方面的计算题,这样的题目一直是中考的热点,主要培养学生的综合分析能力和计算能力

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
7.下列图示是实验的基本操作,其中正确的是( )
| A. |  熄灭酒精灯 | B. | 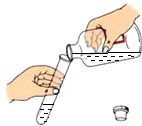 倾倒液体 | C. | 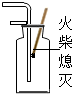 气体验满 | D. |  液体过滤 |
11.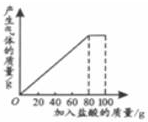 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
(1)第2次加入盐酸后,a为25g.
(2)实验中所用的稀盐酸中,溶质的质量分数是多少?
 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象. | 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(2)实验中所用的稀盐酸中,溶质的质量分数是多少?
14.下列造成空气污染的因素主要由物理变化引起的是( )
| A. | 生活垃圾焚烧产生的有害气体 | B. | 建筑施工导致尘土飞扬 | ||
| C. | 生物腐烂放出的一氧化碳 | D. | 煤燃烧产生的刺激性气味气体 |