题目内容
某化验员取纯碱样品(含氯化钠)44g于烧杯中加水将其溶解,然后分几次逐滴加入溶质质量分数为20%的稀盐酸,并不断搅拌,称量,将得到的有关数据记录如下:(注:加盐酸时首先发生反应是:Na2CO3+HCl=NaHCO3+NaCl,然后是NaHCO3+HCl=NaCl+CO2↑+H2O)
| 加入稀盐酸质量/g | 0 | 73 | 74 | 146 | 147 |
| 烧杯中溶液质量/g | 200 | 273 | 273.76 | 328.4 | 329.4 |
(1)加入 g稀盐酸开始产生二氧化碳.
(2)计算恰好不再产生气体时,所得溶液的溶质质量分数.(保留一位小数)
| (1)分析图表中溶液质量变化可知,加入73克稀盐酸时,烧杯中溶液质量273克,说明没有气体放出;在74克时,溶液质量有变化,说明开始产生二氧化碳; (2)根据加入147克和加入146克时溶液质量比较,可以发现多加1克盐酸,溶液的质量也增加1克,说明加入146克稀盐酸时样品中碳酸钠完全反应,不再产生气体; 样品中碳酸钠完全反应,依据质量守恒定律减少的质量即是生成二氧化碳的质量,结合化学方程式计算生成氯化钠的质量,然后据溶液中溶质的质量分数分析解答. | |
| 解答: | 解:(1)加入73克稀盐酸开始产生二氧化碳,因为加入73克稀盐酸时,烧杯中溶液质量为200+73=273克,此时总体积没有减少,因此没有气体产生; 而加入74克稀盐酸时,质量减少了0.24克,说明加入大于73克稀盐酸时开始产生二氧化碳; (2)加入147克时溶液质量为329.4克,加入146克时溶液质量为328.4克,此时多加1克盐酸,烧杯中溶液的质量也是增加1克,说明样品中碳酸钠完全反应,因此没有气体产生,共放出二氧化碳为:146g+200g﹣328.4g=17.6g; 设样品中Na2CO3的量为x,生成氯化钠的质量为y Na2CO3+2HCl=2NaCl+H2O+CO2↑ 106 117 44 x y 17.6g
x=42.4g
y=46.8g 那么样品中NaCl的质量为44g﹣42.4g=1.6g 所得氯化钠溶液的质量分数是: 故答案为:(1)大于73;(2)恰好不再产生气体时,所得溶液的溶质质量分数14.7%. |

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案某化验员取纯碱样品(含氯化钠)44g于烧杯中加水将其溶解,然后分几次逐滴加入溶质质量分数为20%的稀盐酸,并不断搅拌,称量,将得到的有关数据记录如下:(注:加盐酸时首先发生反应是:Na2CO3+HCl=NaHCO3+NaCl,然后是NaHCO3+HCl=NaCl+CO2↑+H2O)
| 加入稀盐酸质量/g | 0 | 73 | 74 | 146 | 147 |
| 烧杯中溶液质量/g | 200 | 273 | 273.76 | 328.4 | 329.4 |
(2)计算恰好不再产生气体时,所得溶液的溶质质量分数.(保留一位小数)
| 加入稀盐酸质量/g | 73 | 74 | 146 | 147 | |
| 烧杯中溶液质量/g | 200 | 273 | 273.76 | 328.4 | 329.4 |
(2)计算恰好不再产生气体时,所得溶液的溶质质量分数.(保留一位小数)
某化验员取纯碱样品(含氯化钠)44g于烧杯中加水将其溶解,然后分几次逐滴加入溶质质量分数为20%的稀盐酸,并不断搅拌,称量,将得到的有关数据记录如下:(注:加盐酸时首先发生反应是:Na2CO3 + HCl = NaHCO3 + NaCl ,然后是NaHCO3 + HCl = NaCl + CO2↑+ H2O)
(1)加入 g稀盐酸开始产生二氧化碳。
(2)计算恰好不再产生气体时,所得溶液的溶质质量分数。(保留一位小数)
| 加入稀盐酸质量/g | 0 | 73 | 74 | 146 | 147 |
| 烧杯中溶液质量/g | 200 | 273 | 273.76 | 328.4 | 329.4 |
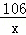 =
=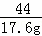
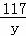 =
=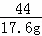
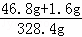 ×100%≈14.7%
×100%≈14.7%