题目内容
5.人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用,请回答下列问题:(1)智能手机给我们的生活带来了很大的变化,制作其充电线的主要原料是铜,这是利用了铜的延展性和导电性.(2)钢铁的锈蚀给人类打来了巨大的损失,铁生锈是因为铁与空气中的氧气、水等发生了化学反应,废旧钢铁表面的铁锈可用盐酸除去,其化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(3)锰和镍(Ni)都是重要的金属,将镍丝插入MnSO4溶液中,无明显现象,插入CuSO4溶液中,镍丝表面有红色固体析出,则Mn、Ni、Cu三种金属活动性由强到弱的顺序是Mn>Ni>Cu.
(4)在托盘天平左、右两边各放一只质量相等的烧杯,在两只烧杯中加入等质量、等浓度的稀盐酸,此时天平保持平衡,然后向左盘烧杯中加入5g锌粒,向右盘烧杯中加入5g铁粉,充分反应后,两烧杯底部均有固体剩余,则此时天平平衡(填“平衡”或“不平衡”).
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸有气泡产生,则滤渣中一定含有的物质是铜、铁,滤液中一定不含有的物质是硫酸、硫酸铜.
分析 (1)根据金属的性质和用途进行分析.
(2)根据铁生锈的原理以及化学方程式的书写方法进行分析.
(3)根据金属活动性顺序的应用分析判断.排在前面的金属能把排在后面的金属从它的盐溶液中置换出来.
(4)根据题中信息结合金属的化学性质进行分析.
(5)根据在金属活动性顺序中,排在氢前面的金属,能够和稀盐酸、稀硫酸发生置换反应,生成氢气和相应的盐;排在金属活动性顺序前面的金属,能够把排在后面的金属从它的盐溶液中置换出来进行分析.
解答 解:(1)制作其充电线的主要原料是铜,这是利用了铜的延展性和导电性,故填:导电.
(2)铁易与空气中的氧气和水作用形成铁锈.稀盐酸除去铁锈的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.故填:氧气、水;Fe2O3+6HCl=2FeCl3+3H2O.
(3)由题意可知,将镍丝插入MnSO4溶液中,无明显现象,说明锰比镍活泼;将插入CuSO4溶液中,镍丝表面有红色固体析出,说明镍比铜活泼.则Mn、Ni、Cu的活动性由强到弱的顺序是Mn>Ni>Cu,故填:Mn>Ni>Cu.
(4)充分反应后,两烧杯底部均有固体剩余,说明酸完全发生了反应,又因为两只烧杯中加入的是等质量、等浓度的稀盐酸,因此充分反应后生成氢气的质量相同,天平平衡,故填:平衡.
(5)根据“在金属活动性顺序里,排在氢前面的金属能与酸反应产生氢气”这一理论,结合题意中的“向滤渣中加盐酸有气泡产生”可以断定反应后的滤渣中的成分是铁或者锌、铁的混合物,一定有铁生成,锌与硫酸亚铁、硫酸铜的混合溶液反应,先置换出铜,因此有铁一定有铜,所以滤渣中一定含有的固体是铁、铜;因为滤渣中存在铁,因此滤液中一定不含的物质是硫酸、硫酸铜,因为不能和铁共存.
故答案为:铜、铁;硫酸、硫酸铜.
点评 此题综合性较强,主要考查了金属的物理性质和化学性质,是一道不错的题目.

 ”表示氮原子,下列方框中,符合2N2的示意图是( )
”表示氮原子,下列方框中,符合2N2的示意图是( )| A. | 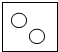 | B. |  | C. | 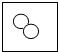 | D. | 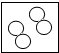 |
| A. | 表示分子个数的是② | |
| B. | 表示离子所带电荷数的是②⑤ | |
| C. | 表示化合价数值的是⑥ | |
| D. | 表示一个分子中所含某种原子个数的是①④ |
| A. | 氧气和氮气-燃着的木条 | B. | 氯化钠和硝酸铵-用水 | ||
| C. | 锌片和银片-硫酸铜溶液 | D. | 碳酸钠粉末和碳酸钙粉末-稀盐酸 |
| A. | CH4 | B. | C2H6S | C. | C4H4S | D. | C6H6S |
| A. | 洁净的空气 | B. | 精制的食盐水 | C. | 冰水混合物 | D. | 澄清石灰水 |