题目内容
18.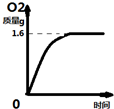 过氧化氢溶液长期保存会自然分解,使溶液的质量分数减小.小军从家中拿来一瓶久置的过氧化氢溶液,和同学们一起测定其溶质质量分数,他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间额关系如图所示.则:
过氧化氢溶液长期保存会自然分解,使溶液的质量分数减小.小军从家中拿来一瓶久置的过氧化氢溶液,和同学们一起测定其溶质质量分数,他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间额关系如图所示.则:(1)完全反应生成氧气的质量为1.6g.
(2)计算过氧化氢溶液的质量分数.
分析 (1)由图示可知,完全反应后生成气体的质量为1.6g;
(2)根据过氧化氢溶液分解的化学方程式和生成氧气的质量,可计算出参与反应的过氧化氢的质量,然后根据质量分数公式计算即可.
解答 解:(1)由图可知完全反应后生成氧气的质量为1.6g;
(2)设参与反应的过氧化氢的质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}$=$\frac{32}{1.6g}$
x=3.4g
该溶液中溶质的质量分数为:$\frac{3.4g}{51g}$×100%=6.7%.
故答案为:(1)1.6g;
(2)该溶液中溶质的质量分数为6.7%.
点评 本题主要考查学生运用化学方程式和溶质的质量分数公式进行计算的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.关于O2,CO2,SO2三种物质的叙述中,正确的是( )
| A. | 都是氧化物 | B. | 都含氧分子 | C. | 都含氧元素 | D. | 都含氧气 |
3.下列变化属于化学变化的是( )
| A. | 轮胎爆炸 | B. | 电灯通电发亮 | C. | 葡萄酿成酒 | D. | 矿石粉碎 |
7.下列物质中,能使溶液中的石蕊变红的是( )
| A. | 二氧化碳 | B. | 酒精 | C. | 甲醇 | D. | 醋酸 |
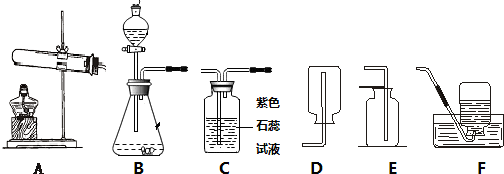
 某同学用如图方法用红磷测定空气中氧气的含量的实验,实验步骤如下:
某同学用如图方法用红磷测定空气中氧气的含量的实验,实验步骤如下: