��Ŀ����
13����֪CO2ͨ�����ʯ��ˮ�У���Һ����ǣ�����ͨCO2�����ɻ����ֱ���壬CaCO3+H2O+CO2�TCa��HCO3��2���ɴ�ij��ѧ��ȤС����̽��CO2��NaOH��Һ��Ӧ���������ɣ���������⡿CO2��NaOH��Һ��Ӧ����������
���������ϡ��١�NaHCO3+NaOH�TNa2CO3+H2O
�ڡ��������̼������Һ�У�ʵ�ʷ�Ӧ����������
��һ����Ӧ��Na2CO3+HCl�TNaCl+NaHCO3
�ڶ�����Ӧ��NaHCO3+HCl�TNaCl+H2O+CO2��
��������롿����1������ΪNa2CO3
����2������ΪNa2CO3��NaOH���ѧʽ������ͬ��
����3������ΪNaHCO3��Na2CO3
����4������ΪNaHCO3
��ʵ�鷽���������ͬѧΪȷ��CO2��NaOH��Һ��Ӧ��������Һ��������ɣ��������ʵ�鷽����
��1����������Һ�м���������CaCl2��Һ�����а�ɫ�������ɣ����˺�����Һ�м���������ϡ���������ݲ�����������ΪNa2CO3��Na2CO3��NaOH��
��2����������Һ�м���������CaCl2��Һ�����ް�ɫ�������ɣ���Һ�м���������ϡ���������ݲ�����������ΪNaHCO3��
��3����������Һ�м���������CaCl2��Һ�����а�ɫ�������ɣ����˺�����Һ�м���������ϡ���������ݲ�����������ΪNaHCO3��Na2CO3��
������ͬѧ���ݼ���ͬѧ�IJ��룬ͨ�������������Ƴ���������Һ����μ���ϡ��������������ɶ�����̼��������ϵʾ��ͼ�������ͼ��ȷ�����ʳɷ֣�
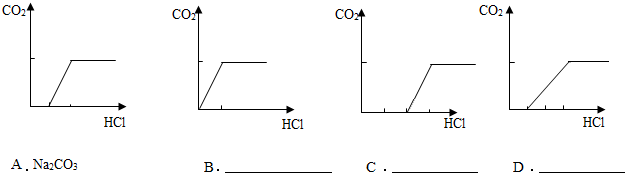
���� ���������ϡ�����CO2ͨ�����ʯ��ˮ�У���Һ����ǣ�����ͨCO2�����ɻ����ֱ���壬CaCO3+H2O+CO2=Ca��HCO3��2��������ȷ�����
��ʵ�鷽��������CaCO3Ϊ��ɫ������Ca��HCO3��2���ܣ�̼���κ�̼�����ζ�������ϡ���ᷴӦ���ɶ�����̼���������
��� �⣺���������ϡ�CO2��NaOH��Һ��Ӧ����Ϊ�ٶ�����̼���㣬��Ӧ����������ΪNa2CO3��ʣ���NaOH����CO2��NaOH��Һ��Ӧ����Na2CO3����Ӧ����������ΪNa2CO3���۶�����̼�Թ��������ڲ���Na2CO3��Ӧ����NaHCO3����Ӧ����������ΪNaHCO3��Na2CO3���ܶ�����̼����������ȫ��Na2CO3��Ӧ����NaHCO3����Ӧ����������ΪNaHCO3��
��ʵ�鷽������1����������Һ�м���������CaCl2��Һ�����а�ɫ�������ɣ�˵����Һ�к���Na2CO3�������Ѿ������������˺�����Һ�м���������ϡ���������ݲ�����˵��û��NaHCO3��������ΪNa2CO3��Na2CO3��NaOH��
��2����������Һ�м���������CaCl2��Һ����û�а�ɫ�������ɣ�˵����Һ��û��Na2CO3�������Ѿ������������˺�����Һ�м���������ϡ���������ݲ�����˵����NaHCO3��������ΪNaHCO3��
��3����������Һ�м���������CaCl2��Һ�����а�ɫ�������ɣ�˵����Һ�к���Na2CO3�������Ѿ������������˺�����Һ�м���������ϡ���������ݲ�����˵����NaHCO3��������ΪNaHCO3��Na2CO3��
������������̼������Һ�У�ʵ�ʷ�Ӧ���������У���һ����Ӧ��Na2CO3+HCl=NaCl+NaHCO3���ڶ�����Ӧ��NaHCO3+HCl=NaCl+H2O+CO2����
Bͼ���Կ������ż����������������������˵������ΪNaHCO3��
Cͼ�Ա�Aͼ��������ֻ��Na2CO3ʱ��������һЩ����������������˵�����ʳ���Na2CO3���NaOH��
Dͼ�Ա�Aͼ��������ֻ��Na2CO3ʱ��������ʱ��������һЩ���ᣬ˵�����ʳ���Na2CO3���NaHCO3��
�ʴ�Ϊ�����������ϡ���Na2CO3��NaOH��NaHCO3��Na2CO3��NaHCO3��
��ʵ�鷽������1��Na2CO3��Na2CO3��NaOH����2��NaHCO3����3��NaHCO3��Na2CO3��
B��NaHCO3��C��Na2CO3��NaOH��D��Na2CO3��NaHCO3��
���� ����Ϊδ֪����ƶϣ���Ҫ������δ֪��ļ��鷽������Ŀ�ѶȽϴ���ȷ�������ʵĻ�ѧ���ʼ����鷽���ǽ���ؼ���

��ȥ���и������л��е��������ʣ������Լ��Ͳ�������ȷ����
ѡ�� | ���� | ���� | �����Լ��Ͳ������� |
A | Na2CO3��Һ | Na2SO4��Һ | ���������Ba(NO3)2��Һ������ |
B | NaCl���� | ϸɳ | ��������ˮ�ܽ⡢���� |
C | H2 | HCl | �ӹ�����NaOH��Һ��Ũ���� |
D | ���� | Fe2O3 | ����������ϡ���ᡢ���ˡ�ϴ�ӡ����� |
A. A B. B C. C D. D
| A�� | ��ΪCO2������ˮ�����Բ�������ˮ���ռ� | |
| B�� | ����ˮ������ֱ���ռ��������Ҹ�������� | |
| C�� | ��Ϊ����ʱNO��O2��Ӧ����NO2�����Բ������ſ������ռ�NO | |
| D�� | ��ΪCO�ж������Բ������ſ������ռ� |
��1��������ͼ�ش����⣮

��A�ǵ��ˮ��ʵ�飬�Թ�1�еõ���������������
��Bͼ�ǻ���̿��ˮ����ʾ��ͼ�����л���̿��������������
��C��Dͼ��̽��������������ʵ�飬һ��ʱ�����C����Ƭ��죬D����Ƭ��Ȼ�������Ա�C��D�е�����˵�����������������һ����Ҫ����������Ũ�ȣ�
��2�����Ϊijͬѧ�ⶨ������ز�ͬ�¶ȵ�ʱ�ܽ�����ݣ�
| �¶ȣ��棩 | 20 | 40 | 50 | 60 | 70 | 80 |
| �ܽ�ȣ�g�� | 31.6 | 63.9 | 85.5 | 110 | 138 | 169 |

�����õ�����Һ�����ʵ���������һ����ȵ���BE������ĸ��ţ���

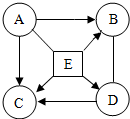 ��֪A��B��C��D��E��Ϊ���л�ѧ�������ᡢ��Ρ����������B�������C���Ȼ��ƣ�E�ڹ�ҵ�Ϲ㷺��Ӧ���ڲ�������ֽ�ȵ����������Ǵ�����ͼ��ʾ��ת����ϵ����֪A��E�ܷ�Ӧ�������壬��ش��������⣨��-����ʾ����ܷ�Ӧ����������ʾ��ij�������������ɸ����ʣ�
��֪A��B��C��D��E��Ϊ���л�ѧ�������ᡢ��Ρ����������B�������C���Ȼ��ƣ�E�ڹ�ҵ�Ϲ㷺��Ӧ���ڲ�������ֽ�ȵ����������Ǵ�����ͼ��ʾ��ת����ϵ����֪A��E�ܷ�Ӧ�������壬��ش��������⣨��-����ʾ����ܷ�Ӧ����������ʾ��ij�������������ɸ����ʣ�