题目内容
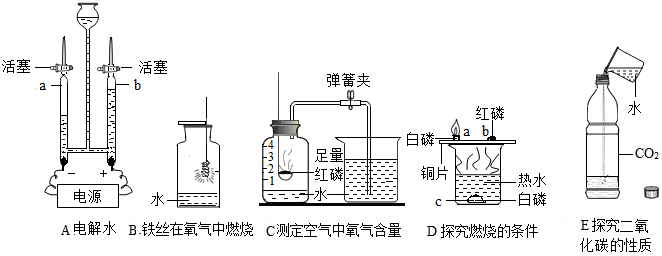
13.碳元素的变化与我们的生活关系密切.(1)下图中C(填编号)表示金刚石的结构,A(填编号)表示C60的分子结构.

(2)每个CO分子比CO2分子少1个氧原子,分子结构的不同造成CO和CO2 的化学性质千差万别.CO分子比CO2中,能使紫色石蕊溶液变红的是CO2,它与水反应的化学方程式是CO2+H2O═H2CO3;能将氧化铜还原成铜的是CO,反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)有研究指出可用地下盐水储存CO2,此过程中涉及到反应2Mg2SiO4+2H2O+CO2═Mg3Si2O5(OH)4+X,则生成物X 为MgCO3(填化学式).生成物Mg3Si2O5(OH)4的相对分子质量为276,其计算式为24×3+28×2+16×9+1×4=276.
分析 根据已有的碳的性质以及构成碳单质和碳的氧化物的知识、质量守恒定律的知识进行分析解答即可.
解答 解:(1)据图可以看出,图中C表示金刚石的结构,A表示C60的分子结构,故填:C,A;.
(2)每个CO分子比CO2分子少1个氧原子,分子结构的不同造成CO和CO2 的化学性质千差万别.CO分子比CO2中,能使紫色石蕊溶液变红的是二氧化碳,它与水反应的化学方程式是CO2+H2O═H2CO3;能将氧化铜还原成铜的是一氧化碳,反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,故填:氧,CO2,CO2+H2O═H2CO3,CO,CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)在反应2Mg2SiO4+2H2O+CO2═Mg3Si2O5(OH)4+X中,反应前含有4个Mg原子,2个Si原子,12个O原子,4个H原子,1个O原子,反应后含有3个Mg原子,2个Si原子,9个O原子,4个H原子,故X中含有一个Mg原子,1个C原子,3个O原子,则生成物X为MgCO3,生成物Mg3Si2O5(OH)4的相对分子质量为276,其计算式为24×3+28×2+16×9+1×4=276.故填:MgCO3,24×3+28×2+16×9+1×4=276.
点评 本题考查的是碳的有关单质和化合物的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.如表列出了除去物质中所含少量杂质的方法,其中正确的是
( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO2气体 | CO气体 | 点燃的方法 |
| B | Fe粉 | Cu粉 | 加入足量稀盐酸至不再产生气泡 |
| C | CaO固体 | CaCO3 | 高温煅烧 |
| D | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
4.下列做法有利于减轻环境污染的是( )
| A. | 将垃圾集中焚烧,以防治雾霾 | |
| B. | 废旧电池深埋土壤中,避免重金属污染 | |
| C. | 火力发电厂加高烟囱,减小废气污染 | |
| D. | 城市加速地铁、轻轨等快速公共交通建设 |
1.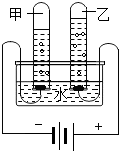 某探究小组用如图电解水
某探究小组用如图电解水
(1)理论上甲管和乙管中产生气体体积比为2:1.
(2)计算:理论上电解3.6克水能生成多少克氧气?(反应的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑)
(3)实际实验记录如下:(装置密闭性良好、读数正确)
实验发现电解开始阶段甲乙两管气体的体积比大于理论比值,你认为可能的原因是AB.(多选)
A.开始阶段产生的O2少量溶解于水
B.电极能与生成的O2反应,而消耗部分氧气
C.生成H2的质量比O2多.
 某探究小组用如图电解水
某探究小组用如图电解水(1)理论上甲管和乙管中产生气体体积比为2:1.
(2)计算:理论上电解3.6克水能生成多少克氧气?(反应的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑)
(3)实际实验记录如下:(装置密闭性良好、读数正确)
| 实验时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 甲管中气体体积/mL | 6 | 12 | 20 | 29 | 39 | 49 | 58 | 69 |
| 乙管中气体体积/mL | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 34 |
A.开始阶段产生的O2少量溶解于水
B.电极能与生成的O2反应,而消耗部分氧气
C.生成H2的质量比O2多.
8.下列说法正确的是( )
| A. | 煤、石油、天然气等化石燃料是人类理想的能源 | |
| B. | 煤是复杂的混合物,主要含有碳元素 | |
| C. | 石油炼制后可得到汽油、柴油、原油等产品 | |
| D. | 天然气就是甲烷(CH4) |
18.SO2气体不是酸,但能与水反应生成酸.请仿照CO2的性质实验,设计实验予以证明.
| 实验操作 | 现象 | 结论 |
| 将干燥的紫色石蕊纸花放入盛有二氧化硫的集气瓶内 | 纸花不变色 | SO2 不是酸 |
| 将湿润的紫色石蕊纸花放入盛有二氧化硫的集气瓶内 | 纸花变红 | SO2 能与水反应生成酸 |
3.下列各组物质是按单质、氧化物、混合物的顺序排列的是( )
| A. | 氧气、水、空气 | B. | 铁粉、干冰、冰水混合物 | ||
| C. | 液氮、氯酸钾、钢 | D. | 石墨、稀有气体、石油 |