题目内容
8.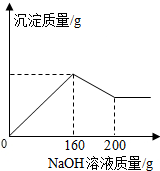 已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O.现有160.0g某无色溶液,可能含有盐酸、硫酸镁、硝酸钾、硫酸铜、氯化铝、碳酸钠中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.
已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O.现有160.0g某无色溶液,可能含有盐酸、硫酸镁、硝酸钾、硫酸铜、氯化铝、碳酸钠中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.(1)推断在该溶液中一定存在的物质是氯化铝、硫酸镁,一定不存在的物质是盐酸、硫酸铜、碳酸钠.
(2)计算原溶液中一种溶质的质量分数.
分析 (1)该溶液为无色,说明一定不含硫酸铜;观察图象,当加入160g氢氧化钠溶液时沉淀质量达到最大,后来逐渐减小,根据题意:氢氧化铝和氢氧化钠可发生反应,说明该溶液中一定含有氯化铝;先生成氢氧化铝,后来氢氧化铝与氢氧化钠发生反应使沉淀减少,沉淀并未全部反应完,说明还含有其他沉淀;
而沉淀从原点开始,说明溶液中一定不含盐酸,因为盐酸可与生成的氢氧化铝发生反应;剩余物质中,硫酸镁可与氢氧化钠反应生成氢氧化镁沉淀,碳酸钠、硝酸钾不与氢氧化钠反应,故一定含有硫酸镁,碳酸钠和硫酸镁会结合生成微溶性的碳酸镁,故二者不能共存,所以溶液中一定不含碳酸钠,可能含有硝酸钾;
(2)由图象可知,当加入160g氢氧化钠溶液时沉淀质量达到最大,说明溶液中物质全部参加反应,后来沉淀减少,说明与氢氧化铝反应的氢氧化钠溶液为200g-160g=40g,据此计算生成氢氧化铝的质量,再由氢氧化钠与氯化铝反应的方程式计算氯化铝的质量.
解答 解:(1)该溶液为无色,说明一定不含硫酸铜;观察图象,当加入160g氢氧化钠溶液时沉淀质量达到最大,后来逐渐减小,根据题意:氢氧化铝和氢氧化钠可发生反应,说明该溶液中一定含有氯化铝;先生成氢氧化铝,后来氢氧化铝与氢氧化钠发生反应使沉淀减少,沉淀并未全部反应完,说明还含有其他沉淀;而沉淀从原点开始,说明溶液中一定不含盐酸,因为盐酸可与生成的氢氧化铝发生反应;剩余物质中,硫酸镁可与氢氧化钠反应生成氢氧化镁沉淀,碳酸钠、硝酸钾不与氢氧化钠反应,故一定含有硫酸镁,碳酸钠和硫酸镁会结合生成微溶性的碳酸镁,故二者不能共存,所以溶液中一定不含碳酸钠,可能含有硝酸钾;
(2)由图象可知,当加入160g氢氧化钠溶液时沉淀质量达到最大,说明溶液中物质全部参加反应,后来沉淀减少,说明与氢氧化铝反应的氢氧化钠溶液为200g-160g=40g
设生成氢氧化铝的质量为x
Al(OH)3+NaOH=NaAlO2+2H2O
78 40
x 40g×20%
$\frac{78}{x}=\frac{40}{40g×20%}$
x=15.6g
设生成15.6g氢氧化铝需氯化铝的质量为y
AlCl3+3NaOH=Al(OH)3↓+3NaCl
133.5 78
y 7.8g
$\frac{133.5}{y}=\frac{78}{7.8g}$
y=26.7g
原溶液中氯化铝的质量分数为:$\frac{26.7g}{100.0g}$×100%=26.7%
故答案为:(1)氯化铝、硫酸镁;盐酸、硫酸铜、碳酸钠;
(2)原溶液中氯化铝的质量分数为26.7%.
点评 在解此类题时,首先要分析题中图象各个转折点表示的含义,然后根据题中所给的数据和反应方程式列出关系式进行分析解答,了解物质的性质才能正确分析和推断溶液中所含的物质,本题能很好的考查学生依据所学知识分析解决问题的能力.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案| A. | 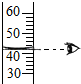 量取液体 | B. | 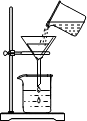 过滤 | C. | 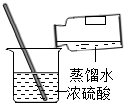 稀释浓硫酸 | D. | 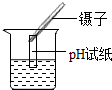 检测溶液pH |
| A. | 金刚石和石墨都是碳的单质,金刚石很硬,故石墨也很硬 | |
| B. | 合金比组成它的纯金属硬,故黄铜比纯铜硬 | |
| C. | 稀硫酸能和氯化钡反应生成白色沉淀,故稀盐酸也可以 | |
| D. | 氢氧化镁和氢氧化钠都是碱,氢氧化镁可以治疗胃酸过多,故氢氧化钠也可以 |
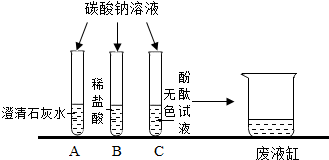
(1)A 中发生反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)B中发生化学反应的实质是氢离子与碳酸根离子反应生成水分子和二氧化碳分子.
(3)C中观察到的现象是酚酞试液变红色.
(4)将A、B、C三支试管内反应后的物质倒入废液缸中,发现废液澄清有气泡冒出,且酚酞溶液呈无色.
【提出问题】最终溶液中含有什么溶质?
【猜想与假设】
甲同学的猜想:废液中有氯化钙和氯化钠;
乙同学的猜想:废液中有氯化钙、氯化钠和氯化氢;
【活动与探究】为了验证甲、乙两位同学的猜想请你设计实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量废液于试管中,向其中加入. | 有气泡冒出 | 乙同学猜想正确 |
最终废液的正确处理方法是加入适量熟石灰中和后排放.
| A. | KNO3、HCl、NaNO3 | B. | K2CO3、Ba(NO3)2、NaCl | ||
| C. | KOH、HNO3、NaCl | D. | FeCl3、NaNO3、KCl |
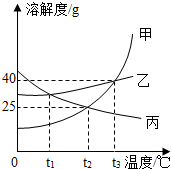 如图为甲、乙、丙三种固体物质的溶解度曲线,请回复.
如图为甲、乙、丙三种固体物质的溶解度曲线,请回复.