题目内容
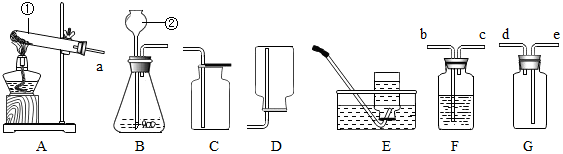
5.现有铁粉、氢氧化铜、铜粉三种固体:硫酸铜、氢氧化钠、硫酸亚铁、硝酸钾、稀硫酸和硫酸钠六种溶液.从中选出适当物质写出符合下列耍求的化学方程式:(1)固体甲+溶液B→溶液E+氢气Fe+H2SO4=FeSO4+H2↑
(2)固体乙+溶液B→溶液C+水Cu(OH)2+H2SO4=CuSO4+2H2O
(3)溶液A+溶液C→固体乙+溶液D2NaOH+CuSO4=Na2SO4+Cu(OH)2↓.
分析 现有铁粉、Cu(OH)2、铜粉三种固体和CuSO4、NaOH、FeSO4、KNO3、Na2SO4、硫酸六种溶液,固体甲+液体B→溶液E+H2↑,结合铁与硫酸反应生成硫酸亚铁和氢气,则甲为铁,B为硫酸,E为硫酸亚铁溶液;固体乙+溶液B→溶液C+H2O,结合硫酸能与氢氧化铜反应生成硫酸铜和水,则乙为氢氧化铜,C为硫酸铜溶液;溶液A+溶液C→固体乙+溶液D,结合氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,则A为氢氧化钠溶液,D为硫酸钠溶液;据此进行分析解答.
解答 解:现有铁粉、Cu(OH)2、铜粉三种固体和CuSO4、NaOH、FeSO4、KNO3、Na2SO4、硫酸六种溶液,固体甲+液体B→溶液E+H2↑,结合铁与硫酸反应生成硫酸亚铁和氢气,则甲为铁,B为硫酸,E为硫酸亚铁溶液;固体乙+溶液B→溶液C+H2O,结合硫酸能与氢氧化铜反应生成硫酸铜和水,则乙为氢氧化铜,C为硫酸铜溶液;溶液A+溶液C→固体乙+溶液D,结合氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,则A为氢氧化钠溶液,D为硫酸钠溶液.
甲为铁,乙为铜.ABCD分别是氢氧化钠溶液、硫酸、Na2SO4溶液.
故答案为:Fe+H2SO4=FeSO4+H2↑;Cu(OH)2+H2SO4=CuSO4+2H2O;2NaOH+CuSO4=Na2SO4+Cu(OH)2↓.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
13.用8g氢氧化钠配制10%的氢氧化钠溶液,需加水的质量为( )
| A. | 102g | B. | 100g | C. | 72g | D. | 无法计算 |
5.下列方法能用来鉴别软水与硬水的是( )
| A. | 观察颜色 | B. | 加肥皂水 | C. | 过滤 | D. | 放一块小木块 |
10.为了减少污染,某工厂用氢氧化钠溶液来吸收工厂烟气中的二氧化硫,反应的化学方程式为:2NaOH+SO2═Na2SO3+X,则X的化学式为( )
| A. | H2 | B. | O2 | C. | H2O | D. | H2O2 |
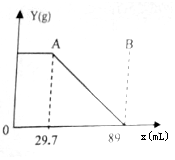 某固体物质由MgSO4和NaOH组成,取24g该固体混合物溶于50g水中,向所得的混合物中逐滴加入15%的硫酸(密度为1.1g.mL),测得沉淀量y与加入的硫酸的体积x有如图表示的关系.
某固体物质由MgSO4和NaOH组成,取24g该固体混合物溶于50g水中,向所得的混合物中逐滴加入15%的硫酸(密度为1.1g.mL),测得沉淀量y与加入的硫酸的体积x有如图表示的关系.