题目内容
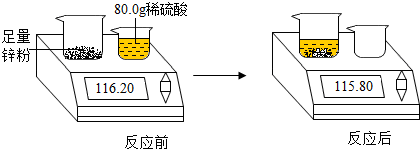
8.测定稀硫酸的溶质质量分数小明为了测定某稀硫酸溶质的质量分数,将80.0g的稀硫酸倒入盛有足量锌粉的烧杯中,恰好完全反应(假设产生的气体全部逸出),实验过程如图所示.
试计算:
(1)根据质量守恒定律,可知生成氢气0.4g;
(2)试计算稀硫酸中溶质的质量分数.
分析 (1)根据质量守恒定律求出生成氢气的质量;
(2)根据锌与稀硫酸的反应,由氢气的质量求出硫酸中溶质的质量,再求出稀硫酸中溶质的质量分数.
解答 解:(1)由质量守恒定律可知,生成氢气的质量为:116.20g-115.80g=0.40g;故填:0.40g;
(2)设稀硫酸中溶质质量为x
Zn+H2S04═ZnS04+H2↑
98 2
x 0.40g
$\frac{98}{2}=\frac{x}{0.40g}$
x=19.6g
稀硫酸中溶质的质量分数=$\frac{19.6g}{80g}×100%$=24.5%.
稀硫酸中溶质的质量分数为24.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
相关题目
19.稀土元素铕(Eu)是激光及原子能应用的重要材料.铕的氧化物的化学式是Eu2O3,其中Eu元素的化合价是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
3.科学家利用太阳能在二氧化铈(CeO2)的催化作用下将H2O、CO2转变成H2、CO和O2.下列有关说法错误的是( )
| A. | 该反应属于置换反应 | |
| B. | 二氧化铈在反应前后质量和化学性质没有改变 | |
| C. | 二氧化铈中铈元素的化合价为+4 | |
| D. | 该反应的产物H2和CO均可作为气体燃料 |
13.下列物质在氧气中燃烧,产生无色有刺激性气味的气体是( )
| A. | 木炭 | B. | 铁丝 | C. | 硫磺 | D. | 红磷 |
20.酸雨的形成主要与下列哪项有关?( )
| A. | 大量使用塑料购物袋 | B. | 工业和生活污水任意排放 | ||
| C. | 大量使用煤作燃料 | D. | 农业生产任意使用农药和化肥 |
17.在2Cu(NO3)2═2CuO+O2+4X↑反应中,X的化学式为( )
| A. | H2 | B. | NO2 | C. | CO2 | D. | NO |