题目内容
13.月球上的23He蕴藏量巨大,地球上的氦元素主要以24He形式存在.从原子的构成来看,23He、24He两种原子的中子数不同,化学性质基本相同,互称为同位素原子.分析 根据相对原子质量≈质子数+中子数判断3He、4He的中子数关系,根据两种原子的电子层结构判断二者的化学性质.
解答 解:23He、24He中的3和4分别是它们的相对原子质量,相对原子质量≈质子数+中子数,氦的原子序数为2,质子数也为2,所以中子数分别为:3-2=1和4-2=2,不相同,由于原子中质子数=核外电子数,所以二者的电子层结构相同,则化学性质相似,二者互称为同位素原子.
故答案为:中子;同位素;
点评 原子的结构及与性质的关系成了考查热点之一,在学习中要注意理论联系实际,运用化学知识去解决实际问题.

练习册系列答案
相关题目
3.如图是某些物品的近似pH,其中酸性最强的是( )
| A. |  猕猴桃 | B. |  醋 | C. |  纯牛奶 | D. | 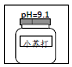 小苏打 |
1.随机取一定量的镁粉和铜粉的混合物于烧杯中,再向其中分次加入同一稀硫酸.实验过程中有关物质的用量及质量测定并记录如下表:
请回答下列问题:
(1)随机所取镁粉和铜粉混合物的质量为9.8克;
(2)第四次实验操作结束后的溶液中溶质的化学式为H2SO4、MgSO4;
(3)所用稀硫酸中溶质的质量分数为多少?
| 实验次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量(克) | 35 | 35 | 35 | 35 |
| 剩余固体的质量(克) | 8.6 | 7.4 | 6.2 | 5.2 |
(1)随机所取镁粉和铜粉混合物的质量为9.8克;
(2)第四次实验操作结束后的溶液中溶质的化学式为H2SO4、MgSO4;
(3)所用稀硫酸中溶质的质量分数为多少?
8.美国首颗“嗅碳”卫星在发射升空过程中因运载火箭出现故障坠毁,这颗卫星的主要任务是绘制全球二氧化碳循环地理分布图.下面关于二氧化碳的叙述不正确的是( )
| A. | 二氧化碳能使澄清的石灰水变浑浊 | |
| B. | 二氧化碳是植物进行光合作用必不可少的原料 | |
| C. | 自然界中的二氧化碳主要消耗途径是植物的呼吸作用 | |
| D. | 固态二氧化碳俗称干冰,升华时可吸收大量热,因而用作制冷剂 |
5.天平两边各放质量相等的烧杯,并分别盛有4.9%的硫酸100克,为了保持天平平衡,可分别往两烧杯中加入( )
| A. | 镁1克、铝1克 | B. | 镁2克、铁2克 | ||
| C. | 锌3.25克、铁2.8克 | D. | 镁3.5克、锌3.5克 |
2.某些非金属氧化物与水反应生成酸,且在这类反应中非金属氧化物中的非金属元素化合价不会发生改变.下列对应关系中符合上述表述的是( )
| A. | CO•H2CO3 | B. | NO2•HNO3 | C. | SO2•H2SO4 | D. | P2O5•H3PO4 |
3.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | N2 | O2 | 将气体缓缓通过足量的灼热焦炭 |
| B | CaO | CaCO3 | 加水溶解、过滤 |
| C | Fe | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |