题目内容
8.下面的实验仪器省去了固定装置,请根据要求回答问题: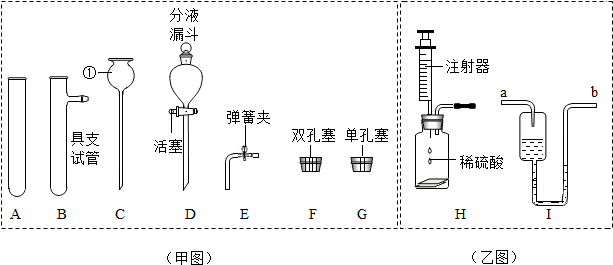
(1)甲图中仪器①的名称为长颈漏斗.
(2)不重复使用,甲图中的仪器可装配两套用于实验室制CO2的装置,它们的组合分别是ADEF、BDG(填序号),制取CO2的化学反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,收集的方法只能用向上排空气法,原因是密度大于空气.若选用分液漏斗装配,其作用相当于乙图中的注射器可以控制滴加液体的速率.
(3)用乙图中的微型装置H可以制少量H2,和I(是医用输液观察滴液快慢的滴壶)相连接还可测量制得的H2体积,但需要补充的仪器是量筒(写名称),此时H2应从a(填“a”或“b”,下同)进入I;若用I作微型洗气装置则气体应从b进入.
分析 (1)根据仪器名称解答;
(2)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.微型装置中用的是注射器,在操作上的优点是:可控制反应速率;在甲图中可选择试管、分液漏斗、带弹簧夹的导管和双孔橡皮塞装配与装置H功能相同的装置;
(3)该装置适用于固液常温下制取气体,I是医用输液观察滴夜快慢的滴壶,若用它作微型洗气装置,则气体应从b进入,其中所装洗气的液体不能装满的原因是液体不会被压往a处流出.
解答 解:(1)①甲图中仪器①的名称是长颈漏斗;故填:长颈漏斗;
(2)在甲图中可选择试管、分液漏斗、带弹簧夹的导管和双孔橡皮塞、单孔塞装配,故甲图中的仪器可装配两套用于实验室制CO2的装置,它们的组合分别是ADEF、BDG;制取CO2的化学反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,收集的方法只能用向上排空气法,原因是CO2密度比空气大,可溶于水.微型装置中用的是注射器,在操作上的优点是:可控制反应速率、节约时间,操作简便、节省试剂;若选用分液漏斗装配,其作用相当于乙图中的注射器,可以控制滴加液体的速率.
(3)用乙图中的微型装置H可以制少量H2,和I(是医用输液观察滴液快慢的滴壶)相连接还可测量制得的H2体积,但需要补充的仪器是量筒,此时H2应从a进入I;若用I作微型洗气装置则气体应从b进入.
故答案为:
(1)长颈漏斗;(2)ACEF;BDG(或ADEF BCG); CaCO3+2HCl═CaCl2+H2O+CO2↑;向上排空气法;CO2密度比空气大,可溶于水;注射器;速率;(3)量筒;a;b
点评 本考点主要考查了仪器的名称;气体的制取装置中仪器的选择,同时也考查了化学方程式的书写,综合性比较强.本考点是中考的重要考点之一,主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| A. | 氧化镁OMg | B. | 碳酸钙caCO3 | C. | 五氧化二氮N2O5 | D. | 一氧化碳Co |
 某校化学兴趣小组就空气中氧气的含量进行实验探究:
某校化学兴趣小组就空气中氧气的含量进行实验探究:【收集资料】硫是一种淡黄色固体,在空气中点燃时能与氧气发生反应生成二氧化硫(表达式:S+O2→SO2).SO2是一种有刺激性气味的气体,易溶于水.
【设计实验】第一小组同学选择的药品是足量的红磷,设计了如图1装置.
(1)红磷在燃烧时的主要现象是发黄光、放出热量、冒出大量的白烟.
(2)燃烧完毕,冷却至室温后打开止水夹,看到的现象是水进入集气瓶约占瓶内空气体积的五分之一.
(3)一般不用木炭的原因是木炭燃烧生成二氧化碳,内外压强变化不大.
(4)集气瓶中红磷燃烧的表达式是磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
| 步骤 | 现象 |
| ①用燃烧匙将硫点燃后伸入到大试管中,立即密封. | 硫燃烧 |
| ②待硫熄灭后,将试管倒立于 盛有冷水的水槽中,并在水中将橡皮塞取下.如图2 | 一段时间后,试管中上升了一段稳定的水柱,水约占试管容积的$\frac{1}{5}$ |
(6)最终水约占试管容积的$\frac{1}{5}$,该实验的结论是氧气约占空气体积的五分之一.
(7)如果不足$\frac{1}{5}$,可能是下列原因中的ABC(填字母).
A.硫用量不足B.未冷却至室温C.气密性不好
(8)取试管中液体放入另一支试管中,在空气中放置一段时间,然后加入紫色石蕊试液,紫色石蕊试液变为红色,说明其中生成了酸性物质--硫酸.请写出硫酸的化学式H2SO4.给它加热,发现它不变为紫色,请你推测硫酸的一个化学性质硫酸受热不易分解.
| A. | 2H-2个氢元素 | B. | 2O2-2个氧分子 | C. | 3Mg2--3个镁离子 | D. | SO4-硫酸 |
| A. | 决定原子质量--质子和电子 | B. | 区别元素种类--质子数 | ||
| C. | 决定元素化学性质--最外层电子数 | D. | 化学变化的实质--原子发生变化 |
| A. |  | B. |  | C. |  | D. |  |