题目内容
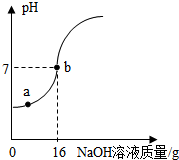 实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如图所示.试回答:
实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如图所示.试回答:(1)a点溶液中含有的溶质有
(2)计算稀H2SO4的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据溶液的pH、稀H2SO4与NaOH溶液的反应分析溶液中存在的离子;
(2)根据稀H2SO4与NaOH溶液的反应的方程式,由NaOH的质量求出稀H2SO4的溶质稀H2SO4的溶质质量分数,
再求出稀H2SO4的溶质质量分数.
(2)根据稀H2SO4与NaOH溶液的反应的方程式,由NaOH的质量求出稀H2SO4的溶质稀H2SO4的溶质质量分数,
再求出稀H2SO4的溶质质量分数.
解答:解:(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以溶液中含有的溶质有:H2SO4、Na2SO4;故答案为:H2SO4、Na2SO4;
(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;
10g稀硫酸样品含有H2SO4的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
0.8g x
=
解得:x=0.98g
稀H2SO4的溶质质量分数为:
×100%=9.8%
答:稀H2SO4的溶质质量分数是9.8%.
(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;
10g稀硫酸样品含有H2SO4的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
0.8g x
| 80 |
| 0.8g |
| 98 |
| x |
解得:x=0.98g
稀H2SO4的溶质质量分数为:
| 0.98g |
| 10g |
答:稀H2SO4的溶质质量分数是9.8%.
点评:此题是一道结合图象的计算题,解题时找到PH=7的恰好反应点,并利用化学方程式的计算进行解决是解题的突破口.

练习册系列答案
相关题目
“安全重于泰山,安全高于一切”.为确保安全、顺利地完成实验任务,每一个实验一定要正确、规范地操作,下列操作正确的是( )
| A、稀释浓硫酸时,将浓硫酸慢慢注入盛水的量筒内 |
| B、用胶头滴管加液体时,把滴管伸入试管内 |
| C、把pH试纸直接浸入待测液中,测定其pH |
| D、把氢氧化钠固体放在天平左盘上的玻璃器皿中称量 |



