题目内容
16.现有50g溶质质量分数为10%的硝酸钾溶液,为使其溶质质量分数增大一倍,应蒸发掉水的质量为25g或加入硝酸钾的质量为6.25g.分析 要使溶液的溶质质量分数变大,常通过两种方式:①加入溶质,②蒸发溶剂,据此结合溶质质量分数的计算进行分析解答.
解答 解:设需要再溶解该物质的质量为x,(50g+x)×20%=50g×10%+x,x=6.25g
设需要蒸发水的质量为y,(50g-y)×20%=50g×10%,y=25g.
即:应向此溶液中加入硝酸钾6.25g,或蒸发掉水25g.
故答案是:25g;6.25g.
点评 本题难度不是很大,考查溶液的浓缩问题,掌握溶液浓缩的方法、原理是正确解答此类题的关键所在.

练习册系列答案
相关题目
19.有一瓶气体,是初中化学常见气体组成,经测定含有碳、氧两种元素,且碳、氧元素的质量比为1:2,关于这瓶气体的组成说法错误的是( )
| A. | 可能由三种气体组成 | B. | 不可能是纯净物 | ||
| C. | 一定存在一氧化碳 | D. | 不可能含有氧气 |
4.水电解过程中一定发生变化的是( )
| A. | 原子质量 | B. | 分子种类 | C. | 元素种类 | D. | 原子种类 |
8.24gMg与65gZn,分别与足量的稀H2SO4反应,得到H2的质量比是( )
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 1:3 |
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: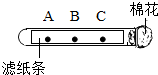 如图所示,将滴有无色酚酞试液的滤纸放在试管中,试管口塞一团棉花.
如图所示,将滴有无色酚酞试液的滤纸放在试管中,试管口塞一团棉花.