题目内容
7.下列知识整理的内容中,均正确的一组是( )| A.物质的鉴别 | B.物质的除杂 |
| 固体(氢氧化钠、氯化钠)--水 溶液(氢氧化钠、盐酸)--酚酞溶液 | 氯化钠中混有少量硫酸铜杂质--氢氧化钡 CO2混有少量CO杂质--点燃 |
| C.物质的用途 | D.物质的分类 |
| 小苏打、碳酸钙--治疗胃酸过多 烧碱、熟石灰--改良酸性土壤 | 纯碱、火碱--碱类 铁、锌、钙元素--人体必需的微量元素 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据氢氧化钠溶于水放出大量的热,溶液温度明显升高,而氯化钠溶于水,溶液温度基本保持不变;氢氧化钠溶液能使酚酞试液变成红色分析;
B、根据氢氧化钡能够和硫酸铜反应产生氢氧化铜沉淀和硫酸钡沉淀、一氧化碳在二氧化碳中不能点燃进行分析;
C、根据氢氧化钠的碱性太强,不能用于改良酸性土壤分析;
D、根据纯碱不是碱,而是盐;钙元素属于常量元素分析.
解答 解:A、氢氧化钠溶于水放出大量的热,溶液温度明显升高,而氯化钠溶于水,溶液温度基本保持不变,因此用水可以鉴别;氢氧化钠溶液能使酚酞试液变成红色,而盐酸不能使酚酞变色,可以鉴别;故选项正确;
B、氢氧化钡能够和硫酸铜反应产生氢氧化铜沉淀和硫酸钡沉淀,能够除去杂质;一氧化碳在二氧化碳中不能点燃,不能用于除去一氧化碳;故选项错误;
C、氢氧化钠的碱性太强,不能用于改良酸性土壤,故选项错误;
D、纯碱不是碱,而是盐;钙元素属于常量元素,故选项错误;
故选项为:A.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
9.硫酸铵[(NH4)2SO4]是常用的一种化学肥料,某浓度的硫酸铵溶液的pH=5.0.以下说法正确的是( )
| A. | 硫酸铵是一种酸 | |
| B. | 长期施用硫酸铵可能导致土壤酸化 | |
| C. | 硫酸铵溶液能使无色酚酞试液变红色 | |
| D. | 硫酸铵与草木灰等碱性物质混合使用可增强肥效 |
18. 为分析某由氧化铜和铜组成的混合物中氧化铜的质量,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如下表:
为分析某由氧化铜和铜组成的混合物中氧化铜的质量,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如下表:
根据实验及有关数据进行分析与计算:
(1)实验中反应物氧化铜有剩余的是A组.
(2)20g该混合物样品中含氧化铜的质量为16g.
(3)根据A组数据计算所用的稀硫酸溶质的质量分数(写出计算过程)
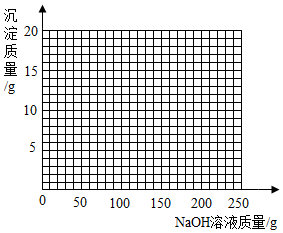
(4)将B组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图.
提示:若溶液中溶质含有H2SO4和CuSO4,则反应的先后顺序如下:
H2SO4+2NaOH=2H2O+Na2SO4
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
 为分析某由氧化铜和铜组成的混合物中氧化铜的质量,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如下表:
为分析某由氧化铜和铜组成的混合物中氧化铜的质量,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如下表:| 组别 | A | B | C |
| 稀硫酸的质量/g | 50 | 100 | 150 |
| 剩余固体的质量/g | 10.0 | 16.0 | 16.0 |
(1)实验中反应物氧化铜有剩余的是A组.
(2)20g该混合物样品中含氧化铜的质量为16g.
(3)根据A组数据计算所用的稀硫酸溶质的质量分数(写出计算过程)
(4)将B组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图.
提示:若溶液中溶质含有H2SO4和CuSO4,则反应的先后顺序如下:
H2SO4+2NaOH=2H2O+Na2SO4
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
15.下列有关生产、环保、能源、资源问题的叙述错误的是( )
| A. | PM2.5专用口罩中使用了活性炭,是利用活性炭的吸附性 | |
| B. | 温室效应主要是由二氧化碳等气体引起的 | |
| C. | 煤、石油、天然气属于混合物,是不可再生能源 | |
| D. | pH<7的雨水说明空气己受到污染 |
16.下列变化中,属于化学变化的是( )
| A. | 玻璃砸碎 | B. | 食物腐烂 | C. | 酒精挥发 | D. | 干冰升华 |
17.下列物质中,属于纯净物的是( )
| A. | 自来水 | B. | 矿泉水 | C. | 白醋 | D. | 蒸馏水 |
 为测定某BaCl2溶液的溶质质量分数,取100g该BaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示.
为测定某BaCl2溶液的溶质质量分数,取100g该BaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示. 合金材料的研究与工业生产的发展关系密切.
合金材料的研究与工业生产的发展关系密切.