题目内容
14.有一种石灰石样品,其中含有的杂质是二氧化硅(二氧化硅是一种不溶于水,不与酸反应,耐高温的固体),某学生想测定该样品的纯度,他取用2g这种石灰石样品,把20g稀盐酸分4次加入,充分反应后剩余固体的质量见下表,问:| 稀盐酸的质量 | 剩余固体的质量 |
| 第1次5g | 1.315g |
| 第2次5g | 0.63g |
| 第3次5g | 0.3g |
| 第4次5g | 0.3g |
(2)石灰石样品中碳酸钙的纯度是多少?
(3)100kg这种纯度的石灰石充分煅烧后,剩余固体的质量为多少kg?(提示:碳酸钙高温煅烧分解成氧化钙和二氧化碳气体)
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
由表中数据可知杂质质量是0.3g;
根据表中提供的数据和反应的化学方程式可以进行相关方面的计算.
解答 解:(1)2克石灰石样品中,有杂质0.3g.
故填:0.3.
(2)石灰石样品中碳酸钙的质量分数为:$\frac{2g-0.3g}{2g}$×100%=85%,
故填:85%.
(3)解:设该石灰石能产生二氧化碳的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
100kg×85% x
$\frac{100}{100kg×85%}=\frac{44}{x}$,
x═37.4kg,
剩余固体的质量为:100kg-37.4kg=62.6kg
答:剩余固体的质量为62.6kg.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
5.下列实验操作中正确的是( )
| A. | 用焰心加热试管,以保证热效率 | |
| B. | 将鼻孔凑到容器口去闻药品的气味 | |
| C. | 蒸发过程中,当蒸发皿中出现较多固体时就应停止加热 | |
| D. | 过滤中,为加快过滤速度,可用玻璃棒在漏斗内搅拌 |
19.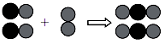 如图是用来表示物质间发生化学变化的模型,图中“
如图是用来表示物质间发生化学变化的模型,图中“ ”、“
”、“ ”分别表示两种不同元素的原子.从示意图中获取的信息正确的是( )
”分别表示两种不同元素的原子.从示意图中获取的信息正确的是( )
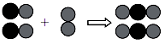 如图是用来表示物质间发生化学变化的模型,图中“
如图是用来表示物质间发生化学变化的模型,图中“ ”、“
”、“ ”分别表示两种不同元素的原子.从示意图中获取的信息正确的是( )
”分别表示两种不同元素的原子.从示意图中获取的信息正确的是( )| A. | 该反应可能是2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | 反应前后原子的种类和个数发生变化 | |
| C. | 生成物分子中两种原子个数比为1:2 | |
| D. | 该反应是分解反应 |
6.下列材料属于金属的是( )
| A. | 玻璃 | B. | 合成橡胶 | C. | 铁 | D. | 陶瓷 |
4.自然科学兴趣小组的同学在整理化学试剂时,发现有三瓶无色溶液失去标签,从实验老师处得知它们分别是稀盐酸、氯化钡溶液、碳酸钠溶液.同学们认为可以用多种方法进行鉴别,通过实验设计并进行实验,它们给这三瓶溶液重新贴上标签.下面是它们设计和实施的两种方案,请你一起参与实验.
(1)方案一:不用其它试剂进行鉴别将三瓶无色溶液任意编号为A、B、C、,各取少量进行实验得到相关的实验记录(见表).
请判断B是稀盐酸溶液;
写出A与C反应的化学方程式BaCl2+Na2CO3=2NaCl+BaCO3↓
(2)方案二:选用其它试剂进行鉴别(请补充实验步骤②).
①用三支试管分别取少量无色溶液;②滴加碳酸钾溶液(等合理即可).
③观察实验现象; ④得出结论.
(1)方案一:不用其它试剂进行鉴别将三瓶无色溶液任意编号为A、B、C、,各取少量进行实验得到相关的实验记录(见表).
| 实验内容 | 观察到的现象 |
| A+B | 有气泡产生 |
| A+C | 有白色沉淀产生 |
写出A与C反应的化学方程式BaCl2+Na2CO3=2NaCl+BaCO3↓
(2)方案二:选用其它试剂进行鉴别(请补充实验步骤②).
①用三支试管分别取少量无色溶液;②滴加碳酸钾溶液(等合理即可).
③观察实验现象; ④得出结论.

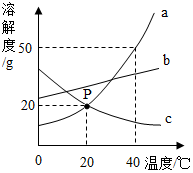 请根据如图所示的a、b、c三种物质的溶解度曲线回答下列问题:
请根据如图所示的a、b、c三种物质的溶解度曲线回答下列问题: