题目内容
近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如图所示.下列说法错误的是( )
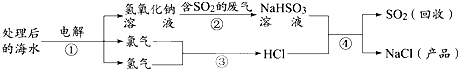

| A、可循环利用的物质是SO2 |
| B、图中反应①属于分解反应 |
| C、反应中硫元素的化合价未发生变化 |
| D、从海水中最终得到“NaCl(产品)”的过程是化学变化 |
考点:酸雨的产生、危害及防治,有关元素化合价的计算,化学变化和物理变化的判别,反应类型的判定
专题:化学与环境保护
分析:A、根据反应物和生成物中都有二氧化硫判断;
B、根据处理后的海水中含有氯化钠和水以及分解反应的定义判断;
C、根据化合物中各元素的化合价代数和为零判断;
D、根据每一步都有新物质生成判断.
B、根据处理后的海水中含有氯化钠和水以及分解反应的定义判断;
C、根据化合物中各元素的化合价代数和为零判断;
D、根据每一步都有新物质生成判断.
解答:解:
A、反应物和生成物中都有二氧化硫,所以可以循环利用,故A正确;
B、根据生成物为氢氧化钠溶液、氯气、氢气,海水为反应物,则可在化学反应式是2NaCl+2H2O
2NaOH+Cl2↑+H2↑,不符合分解反应的定义,故B错误;
C、反应物二氧化硫中硫元素的化合价是+4价,化合物中硫元素的化合价还是+4价,化合价没有发生变化,故C正确;
D、从海水最终得到NaCl(产品)的过程可知,每一步都有新物质生成,为化学变化,故D正确.
答案:B
A、反应物和生成物中都有二氧化硫,所以可以循环利用,故A正确;
B、根据生成物为氢氧化钠溶液、氯气、氢气,海水为反应物,则可在化学反应式是2NaCl+2H2O
| ||
C、反应物二氧化硫中硫元素的化合价是+4价,化合物中硫元素的化合价还是+4价,化合价没有发生变化,故C正确;
D、从海水最终得到NaCl(产品)的过程可知,每一步都有新物质生成,为化学变化,故D正确.
答案:B
点评:解题时往往需要从题目中挖出一些明显或隐含的条件,根据图示提供的信息,抓住突破口(突破口往往是现象特征、反应特征及结构特征),对各个选项逐一分析.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
镁带在氧气中燃烧是化学变化,判断的主要依据是( )
| A、出大量的热 |
| B、看到耀眼的白光 |
| C、有白色粉末成 |
| D、镁带消失 |
化学上称“原子是化学变化中的最小粒子”的根据是( )
| A、原子的体积极小 |
| B、原子在化学反应中不可再分 |
| C、原子的质量极小 |
| D、原子是构成物质的最小粒子 |
对下列符号含义的理解正确的是( )
| A、2H:1个氢分子 |
| B、2O2-:两个氧离子带两个单位负电荷 |
| C、Mg2+:1个镁离子 |
| D、N2:2个氮原子 |