题目内容
(1)根据图1实验示意图回答问题:①实验A中的实验现象是______,写出反应的化学方程式______ Fe3O4

【答案】分析:(1)根据铁丝的燃烧以及二氧化碳的性质分析,
(2)根据双氧水的性质进行分析,根据氧化钙与水的反应以及氢氧化钙的溶解度的变化进行分析,
(3)根据具体的选项结合已有的知识分析.
解答:解:(1)①铁丝在氧气中燃烧火星四射,放出大量的热,反应后有黑色固体生成,该物质是四氧化三铁,该反应属于化合反应,故填:火星四射,放出大量的热,有黑色物质生成; 3Fe+2O2 Fe3O4;化合反应;
Fe3O4;化合反应;
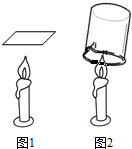
②二氧化碳使阶梯蜡烛熄灭的实验说明二氧化碳既不燃烧也不支持燃烧,故填:二氧化碳不支持燃烧;二氧化碳也不燃烧;
③电解水实验中生成的氧气和氢气的体积比为1:2,故填:1:2;
(2)①过氧化氢在二氧化锰的催化作用下能生成水和氧气,B中的氧化钙能与水反应生成氢氧化钙,故填:2H2O2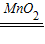 2H2O+O2↑;氧化钙;
2H2O+O2↑;氧化钙;
②过氧化氢分解生成的氧气使瓶内的压强增大,U形管内右侧的液面升高,能使液体流入C装置,故填:U形管内右侧的液面升高,管内液体流向装置C;
③氧化钙能与水反应放出大量的热,氢氧化钙的溶解度随温度的升高而减小,会析出氢氧化钙固体而使溶液浑浊,氧化钙与水反应,导致溶液中的溶剂减少,氢氧化钙析出,故填:氧化钙与水反应生成氢氧化钙且放热,温度升高使氢氧化钙的溶解度降低,部分氢氧化钙固体析出;氧化钙与水反应,水被消耗,部分氢氧化钙析出(合理给分)
④装置B、C中白色浑浊是析出的固体氢氧化钙,装置B可以起到贮存气体的作用,反应前后装置B中溶质的质量分数可能不变,故填:BC.
点评:本题考查了常见物质的性质以及有关实验的描述,完成此题,可以依据已有的知识进行.
(2)根据双氧水的性质进行分析,根据氧化钙与水的反应以及氢氧化钙的溶解度的变化进行分析,
(3)根据具体的选项结合已有的知识分析.
解答:解:(1)①铁丝在氧气中燃烧火星四射,放出大量的热,反应后有黑色固体生成,该物质是四氧化三铁,该反应属于化合反应,故填:火星四射,放出大量的热,有黑色物质生成; 3Fe+2O2
 Fe3O4;化合反应;
Fe3O4;化合反应;②二氧化碳使阶梯蜡烛熄灭的实验说明二氧化碳既不燃烧也不支持燃烧,故填:二氧化碳不支持燃烧;二氧化碳也不燃烧;
③电解水实验中生成的氧气和氢气的体积比为1:2,故填:1:2;
(2)①过氧化氢在二氧化锰的催化作用下能生成水和氧气,B中的氧化钙能与水反应生成氢氧化钙,故填:2H2O2
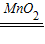 2H2O+O2↑;氧化钙;
2H2O+O2↑;氧化钙;②过氧化氢分解生成的氧气使瓶内的压强增大,U形管内右侧的液面升高,能使液体流入C装置,故填:U形管内右侧的液面升高,管内液体流向装置C;
③氧化钙能与水反应放出大量的热,氢氧化钙的溶解度随温度的升高而减小,会析出氢氧化钙固体而使溶液浑浊,氧化钙与水反应,导致溶液中的溶剂减少,氢氧化钙析出,故填:氧化钙与水反应生成氢氧化钙且放热,温度升高使氢氧化钙的溶解度降低,部分氢氧化钙固体析出;氧化钙与水反应,水被消耗,部分氢氧化钙析出(合理给分)
④装置B、C中白色浑浊是析出的固体氢氧化钙,装置B可以起到贮存气体的作用,反应前后装置B中溶质的质量分数可能不变,故填:BC.
点评:本题考查了常见物质的性质以及有关实验的描述,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
 英国科学家法拉第在《蜡烛的故事》系列讲座中,对蜡烛燃烧所涉及的知识进行了全面介绍.生产蜡烛的主要原料是石蜡和少量的硬脂酸添加剂等,现在让我们一起对蜡烛原料的组成元素进行探究.
英国科学家法拉第在《蜡烛的故事》系列讲座中,对蜡烛燃烧所涉及的知识进行了全面介绍.生产蜡烛的主要原料是石蜡和少量的硬脂酸添加剂等,现在让我们一起对蜡烛原料的组成元素进行探究.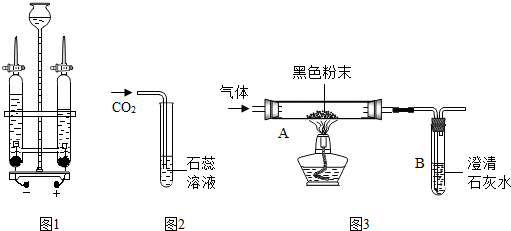
 (1)根据图1实验示意图回答问题:
(1)根据图1实验示意图回答问题: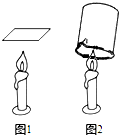 蜡烛是我们生活中的常用品,生产蜡烛的主要原料是石蜡和少量硬脂酸添加剂等,让我们通过实验共同来探究它的组成及有关性质.
蜡烛是我们生活中的常用品,生产蜡烛的主要原料是石蜡和少量硬脂酸添加剂等,让我们通过实验共同来探究它的组成及有关性质.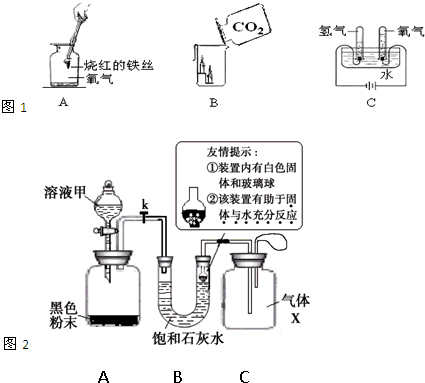 (1)根据图1实验示意图回答问题:
(1)根据图1实验示意图回答问题: