题目内容
11. 化学与生活:
化学与生活:(1)超市通常用加热的方法在塑封食品包装袋,这是应用了塑料的什么性质?但是废弃塑料带来的“白色污染”问题,尤为严重.你能采取什么方法解决这个问题?(答一点)
(2)在探究燃烧的条件实验时,某同学将食品包装袋中的干燥剂(主要成分是生石灰)加入如图水中,一会儿,铜片上的白磷燃烧.请说出产生此现象的原因.
分析 根据塑料的性质、废弃塑料对环境的影响、生石灰与水反应放热以及燃烧的条件进行分析解答即可.
解答 解:(1)超市用加热的方法塑封食品包装袋,这是应用了塑料的热塑性,废弃塑料能造成白色污染,可以将废弃塑料回收利用,故答案为:热塑性;回收各种废弃塑料;
(2)在水中加入生石灰,生石灰能与水反应放出大量的热,使温度达到白磷的着火点,故答案为:生石灰与水反应放热,使温度达到白磷的着火点.
点评 本题考查的是化学与环境、生石灰与水的反应的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2. 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
 三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )| A. | 反应中CaO为催化剂 | B. | 该反应是复分解反应 | ||
| C. | 反应后容器中固体质量减少 | D. | 反应后容器中氧元素质量分数增大 |
19.科学研究表明,氮气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O2$\frac{\underline{\;一定条件\;}}{\;}$2X+6H2O,则X的化学式为( )
| A. | N2 | B. | NO | C. | NO2 | D. | N2O |
6.下列说法错误的是( )
| A. | 质量和质量分数均相等的氢氧化钠溶液与稀硫酸充分反应,所得溶液呈碱性 | |
| B. | 2.3g某物质在空气中完全燃烧,生成4.4g二氧化碳和2.7g水,则该物质一定含有碳、氢两种元素 | |
| C. | 等质量的二氧化硫和三氧化硫,二氧化硫和三氧化硫中硫元素的质量比为5:4 | |
| D. | 足量的镁和锌分别与质量相等、质量分数相等的稀盐酸充分反应,生成氢气的质量相等 |
3.下列关于铁的说法,正确的是( )
| A. | 用水可以除去铁锈 | B. | 铁在潮湿空气中容易生锈 | ||
| C. | 铁生锈不是缓慢氧化 | D. | 铁部分锈蚀后没有回收价值 |
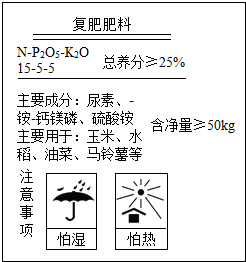 某复合肥的部分说明书如图所示.请回答:
某复合肥的部分说明书如图所示.请回答: