题目内容
19.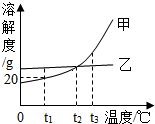 如图是甲、乙两种不含结晶水的固体物质的溶解性曲线.回答下列问题:
如图是甲、乙两种不含结晶水的固体物质的溶解性曲线.回答下列问题:(1)t1℃时,甲物质的溶解度是20g;
(2)当温度为t2℃时,甲、乙物质的溶解度相等;
(3)将等质量甲、乙的两种溶液分别由t3℃降温至t2℃,析出甲的质量>乙的质量大(“>”、“<”、“=”).
分析 根据已有的溶解度曲线的意义进行分析解答,交点表示在该温度下物质的溶解度相等,溶解度随温度升高而增大的物质当升高温度时其溶质质量分数不变;根据溶解度受温度变化的特点确定析出晶体的方法,据此解答.
解答 解:(1)据图可以看出,t1℃时,甲物质的溶解度是20g,故填:20;
(2)据图酷看出,当温度为t2℃时,甲、乙物质的溶解度相等,故填:t2℃;
(3)将等质量甲、乙的两种溶液分别由t3℃降温至t2℃,甲的溶解度受温度影响变化比B大,故析出甲的质量大于乙的质量,故填:>.
点评 本题考查的是溶解度曲线的应用,完成此题,可以依据已有的溶解度曲线的意义进行.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
7.海水蕴藏着丰富的化学资源,目前世界60%的镁是从海水中提取的.其主要流程如图所示.某校兴趣小组同学对从海水中提取金属镁的过程进行了有关探究.
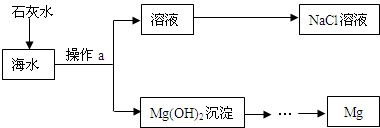
(1)在实验室进行操作a分离后的溶液(海水)中含有CaCl2等杂质,可向其中加入过量的Na2CO3(填化学式,后同)、适量的HCl,蒸发结晶,以除去CaCl2制得较为纯净的NaCl晶体.
(2)兴趣小组同学取一定量的海水样品,分别加入NaOH溶液,进行实验,测得的实验数据如表:
观察与分析上述数据,并计算
①海水样品中氯化镁的质量分数是多少?(计算结果精确到0.001%)
②若从1t这种海水中可提取多少千克金属镁?

(1)在实验室进行操作a分离后的溶液(海水)中含有CaCl2等杂质,可向其中加入过量的Na2CO3(填化学式,后同)、适量的HCl,蒸发结晶,以除去CaCl2制得较为纯净的NaCl晶体.
(2)兴趣小组同学取一定量的海水样品,分别加入NaOH溶液,进行实验,测得的实验数据如表:
| 实验1 | 实验2 | 实验3 | |
| 海水样品质量/g | 100 | 100 | 100 |
| 加入NaOH溶液质量/g | 10 | 15 | 20 |
| 生成沉淀物的质量/g | 0.22 | 0.29 | 0.29 |
①海水样品中氯化镁的质量分数是多少?(计算结果精确到0.001%)
②若从1t这种海水中可提取多少千克金属镁?
4.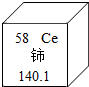 稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )
稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )
 稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )
稀土元素是一类有重要用途的资源,铈是一种常见的稀土元素,下列说法中正确的( )| A. | 铈属非金属元素 | B. | 铈的相对原子质量是140.1克 | ||
| C. | 铈原子的质子数为58 | D. | 铈原子中的中子数为58 |
11.下列生活中的变化,其中涉及化学变化的是( )
| A. | 玉石“变”手镯 | B. | 高粱“变”美酒 | ||
| C. | 树根“变”根雕 | D. | 玩具机器人“变”形 |
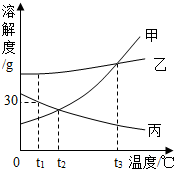 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.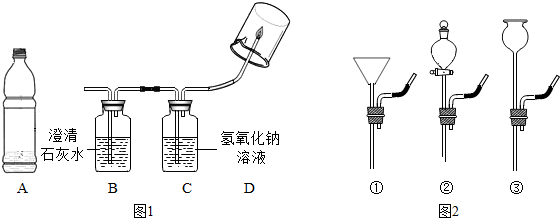
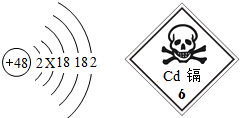 镉(Cd)是一种重金属,镉的毒性较大,被镉污染的空气、食物或饮用水对人体危害严重,应严密监测可能产生隔污染企业的污水排放.隔原子的原子结构示意图和隔物质标签如图,请回答:
镉(Cd)是一种重金属,镉的毒性较大,被镉污染的空气、食物或饮用水对人体危害严重,应严密监测可能产生隔污染企业的污水排放.隔原子的原子结构示意图和隔物质标签如图,请回答: