题目内容
17.如图是甲、乙两种固体物质的溶解度曲线,据图回答: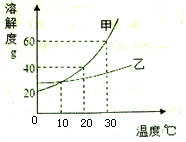
(1)10℃时,甲物质的溶解度=乙物质的溶解度(填“>”或“=”或“<”).
(2)把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,析出晶体较多的是甲.
(3)20℃时,将30g甲物质放入盛有50g水的烧杯中,最终所得溶液为饱和(填“饱和”或“不饱和”)溶液;若将烧杯内物质升温到30℃(不考虑水蒸发),溶液不变的是A(填序号).
A、溶剂的质量 B、溶液的质量 C、溶质的质量分数 D、以上都不变.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,10℃时,甲物质的溶解度=乙物质的溶解度;
(2)30℃时,甲物质的溶解度大于乙物质的溶解度,10℃时,甲、乙物质的溶解度相等,所以把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,析出晶体较多的是甲;
(3)20℃时,甲物质的溶解度是40g,所以将30g甲物质放入盛有50g水的烧杯中,最终所得溶液为饱和溶液,若将烧杯内物质升温到30℃,固体会继续溶解,溶液质量增大,所以溶液中不变的是溶剂的质量,故选:A.
故答案为:(1)=;
(2)甲;
(3)饱和,A.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
8.将6000L氧气在加压下,可装入容积为40L的钢瓶内,这一事实证明( )
| A. | 分子在不断运动 | B. | 分子间有间隔 | C. | 分子的体积很小 | D. | 分子的质量很小 |
5.研究发现,元素原子如果最外层电子数是4,其单质在导电方面具有某些特殊的优良性能,如硅原子最外电子层电子数为4,常用作半导体材料.下列可作半导体材料的是( )
| A. | 铝 Al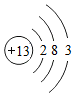 | B. | 氧 O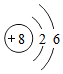 | C. | 锗 Ge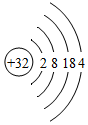 | D. | 氖 Ne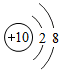 |
12.我国女科学家屠呦呦因发现青蒿素荣获诺贝尔奖医学奖,青蒿素(化学式为C15H22O5)是一种用于治疗疟疾的药物,下列关于青蒿素的说法中正确的是( )
| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 | |
| C. | 青蒿素中氧元素的质量分数最大 | |
| D. | 青蒿素中碳、氢、氧三种原子的个数比为15:22:5 |
2.根据下列三个化学方程式:①Z+Y$\frac{\underline{\;高温\;}}{\;}$2X②2X+O2$\frac{\underline{\;点燃\;}}{\;}$2Z③2CuO+Y$\frac{\underline{\;高温\;}}{\;}$2Cu+Z,试确定X、Y、Z的一组物质是( )
| A. | C、CO、CO4 | B. | CO、CO3、C | C. | C、CO2、CO | D. | CO、C、CO2 |