题目内容
3.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如表所示.他从瓶中倒出200毫升用于配制稀硫酸.求:| 浓硫酸500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)现将200毫升浓硫酸加水稀释,可配制质量分数为19.6%的稀硫酸(密度为1.14克/厘米3)多少毫升?需要水多少毫升?
分析 (1)根据溶液的质量=溶液的体积×溶液的密度来分析;
(2)根据溶液加水稀释过程中,溶液中溶质的质量不变来分析.
解答 解:(1)200毫升=200厘米3,浓硫酸的质量是200厘米3×1.84克/厘米3=368克;故答案为:368克;
(2)设可配制19.6%的稀硫酸的体积为V,则
368g×98%=V×1.14g/cm3×19.6%
V=1614cm3=1614mL
需要水的质量为:1614cm3×1.14g/cm3-368g≈1472g,
即水的体积为1472cm3=1472mL
故答案为:1614mL;1472mL.
点评 本题主要考查了学生对于溶质的质量、溶液的质量及溶质的质量分数之间的关系,以及依据题意计算的能力,要根据题目信息细心分析解答.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
13.有一包白色固体,可能含有CuCl2、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种.为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
| A. | 由①得原白色固体中一定不含CuCl2,一定含量有CaCO3 | |
| B. | 由②③得原白色固体中一定含有Ba(OH)2,一定不含量有Na2SO4 | |
| C. | 由实验现象判断,白色固体中至少有3种固体 | |
| D. | 由实验现象判断,白色固体的组成可有5种情况 |
14. 不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
(1)碳酸钠、碳酸氢钠溶液都能使紫色石蕊试液变成蓝色.
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH增大(填“增大”、“减小”或“不变”),发生反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑.
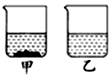
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是Na2CO3(填化学式),加入的质量m的范围为:大于9.6g小于等于21.9g.
 不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示| 温度/℃ | 0 | 20 | 40 | 60 |
| 碳酸钠 | 7.0 | 21.8 | 48.8 | 46.4 |
| 碳酸氢钠 | 6.9 | 9.6 | 12.7 | 16.4 |
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH增大(填“增大”、“减小”或“不变”),发生反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑.
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是Na2CO3(填化学式),加入的质量m的范围为:大于9.6g小于等于21.9g.
11.实验室许多药品需要密封保存.下列药品需密封保存的原因,解释错误的是( )
| A. | 浓盐酸--防止挥发 | B. | NaOH固体--防止其潮解和变质 | ||
| C. | 浓硫酸--防止吸水 | D. | 生石灰--防止与氧气反应 |
18.在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
| A. | 用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码 | |
| B. | 将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液 | |
| C. | 用量筒量取蒸馏水读数时,仰视凹液面的最低处 | |
| D. | 将量筒中的水倒入烧杯时,有水洒出 |
8.将一定量的铁粉放入硝酸铜和硝酸银的混合溶液中,充分反应后过滤,在滤纸上留下少量金属a,并得到滤液b.下列关于a或b的组成说法错误的是( )
| A. | 若向a中滴加稀盐酸有气泡生成,则a中一定含有Fe、Cu、Ag | |
| B. | 若向a中滴加稀盐酸无气泡生成,则b中一定含有Cu2+ | |
| C. | 若向b中滴加稀盐酸无明显变化,则b中一定不含Ag+ | |
| D. | 若向b中滴加稀盐酸产生白色沉淀,则a中一定不含Cu、Fe |
15.下列混合物,属于溶液的是( )
| A. | 牛奶 | B. | 肥皂水 | C. | 钡餐液 | D. | 碘酒 |
12.以下是某同学记录的实验现象,其中错误的是( )
| A. | 镁带在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 在酚酞试液中加入高温煅烧后的石灰石,溶液变蓝 | |
| C. | 在氢氧化钠溶液中滴加硫酸铜溶液,产生蓝色沉淀 | |
| D. | 50mL酒精和50mL水混合后,体积小于100mL |