题目内容
9.随着经济的发展,能源和环境成为人们日益关注的问题.人类目前所消耗的能量主要来自于化石燃料的燃烧.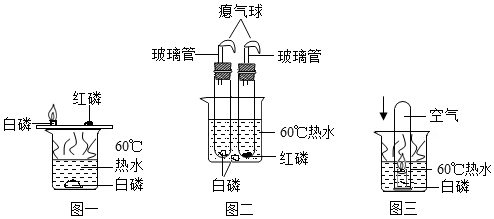
(1)“可燃物燃烧的条件”的实验探究中甲组同学设计了如图一的装置,乙组同学提出磷燃烧生成的大量白烟对人体健康有害,该实验装置必须改进,并设计了如图二的装置,同学们按改进后的图二装置进行实验,实验中观察到的现象是盛白磷的试管中产生大量的白烟,气球先鼓起后变瘪,盛红磷的试管中无现象,于是同学们得出了燃烧的必备条件是可燃物必须与氧气接触,并且温度达到着火点.
(2)同学们用图三再一次证明了“与氧气接触”是可燃物燃烧必备的条件,同时观察到实验中白磷逐渐熄灭后,试管中的液面逐渐上升到接近试管容积的$\frac{1}{5}$处,于是同学们同时也得出了氧气约占空气体积的$\frac{1}{5}$的结论.
(3)“水火不相容”是指水能灭火,请你举出生活实际中用水灭火的实例棉被着火用水浇灭.
分析 根据燃烧的条件分析可得到实验现象的原理;根据空气中氧气的体积约占空气体积的五分之一来分析;根据灭火的原理来分析.
解答 解:(1)通过实验得出了燃烧的必备条件是可燃物必须与氧气接触,并且可燃物的温度需要达到可燃物的着火点;故填:温度达到着火点;
(2)试管中的液面逐渐上升到接近试管容积的$\frac{1}{5}$处,可以得出氧气约占空气体积的$\frac{1}{5}$;故填:氧气约占空气体积的$\frac{1}{5}$;
(3)水蒸发吸热,导致可燃物的温度低于其着火点,而达到灭火的目的.如棉被着火用水浇灭;故填:棉被着火用水浇灭.(合理即可)
点评 熟练掌握物质燃烧的条件,即是:①物质本身具有可燃性,②可燃物与助燃物充分地接触,③达到可燃物的着火点.这三个条件缺一不可,只要同时满足上述三个条件,物质就可以燃烧;同时对于装置优越性的改进一般要考虑到操作的简便性,气密性良好,反应易操控,环境保护等方面.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 高炉炼铁中所需的高温和CO的生成都与焦炭有关 | |
| B. | 液氧可用于火箭发射,是因为氧气具有助燃性 | |
| C. | 碳酸氢铵与氢氧化钙混合使用,既可以增加肥效又可以改良酸性土壤 | |
| D. | 活性炭、Cl2、明矾都可以做净水剂,都可以杀菌 |
 甲、乙两同学在学完酸的化学性质后,做了如下实验:
甲、乙两同学在学完酸的化学性质后,做了如下实验: