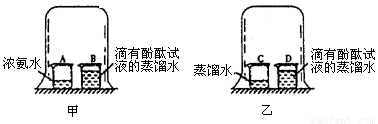题目内容
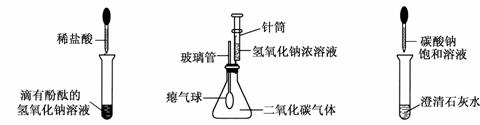
(10分)某兴趣小组在学习碱的化学性质时,进行了如图所示的实验。
(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式 。
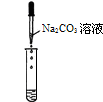
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是 。
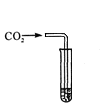
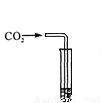
(3)丙实验中观察到试管内有白色沉淀产生。 (4)实验结束后,同学们将甲、乙、丙三个实验的废液倒人同一个子净的废液缸中,最终 看到废液浑浊并呈红色,由此产生疑问。
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和 。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小兰认为:只有碳酸钠
小刚认为:只有氢氧化钙
小亮认为:是氢氧化钠和碳酸钠
你认为还可能是 。(写一种猜想)
【实验设计】小斌想用氯化钙溶液来验证小兰、小刚、小亮的猜想。查阅资料获悉氯化 钙溶液呈中性,并设计如下实验。请你将小斌的实验设计补充完整。
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置。 | ①有白色沉淀,溶液呈红色。 | 的猜想正确。 |
② | 的猜想正确。 | |
③ | 的猜想正确。 |
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑 。
(10分)(1)NaOH+HCl=NaCl+H2O (2)气球胀大
(4)【交流讨论】①NaCl ②氢氧化钠
【实验设计】①小亮 ②有白色沉淀,溶液由红色变为无色 小兰
③没有白色沉淀,溶液呈红色 小刚(实验现象和猜想合理对应即可)
【反思拓展】反应物是否有剩余

10分)某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2; 猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案。另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层澄清溶液于3支试管中。请你参与实验,并填写表中的空白:
| 实验方案 | 方案一 | 方案二 | 方案三 |
| 实验操作 |
|
|
|
| 实验现象 | 澄清溶液变浑浊 | 溶液变 色 |
|
写出方案一中发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意 。
10分)某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2; 猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案。另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层澄清溶液于3支试管中。请你参与实验,并填写表中的空白:
|
实验方案 |
方案一 |
方案二 |
方案三 |
|
实验操作 |
|
|
|
|
实验现象 |
澄清溶液变浑浊 |
溶液变 色 |
|
写出方案一中发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意 。