题目内容
16.将含氧元素质量分数64%的CO和CO2的混合气体1.0g通过足量灼热CuO完全氧化,再使气体通入足量澄清石灰水中,生成白色沉淀的最大质量为( )| A. | 1.0g | B. | 2.0g | C. | 3.0g | D. | 4.0g |
分析 由题意,将含氧元素质量分数64%的CO和CO2的混合气体1.0g通过足量灼热CuO完全氧化,可以计算出混合气体中碳元素的质量,根据质量守恒定律,反应前后碳元素的质量不变,计算出生成白色沉淀的最大质量即可.
解答 解:含氧元素质量分数64%的CO和CO2的混合气体1.0g中含碳元素的质量为1.0g×(1-64%)=0.36g.
质量守恒定律,反应前后碳元素的质量不变,完全反应后生成碳酸钙沉淀的最大质量为0.36g÷($\frac{12}{40+12+16×3}×$100%)=3.0g.
故选:C.
点评 本题难度不大,掌握质量守恒定律(反应前后碳元素的质量不变)、化学式的有关计算是正确解答本题的关键.

练习册系列答案
相关题目
6.对比学习有利于发现事物的共性与个性.为探究酸的性质,同学们进行了如下实验.
【发现问题】碱式碳酸铜与稀硫酸反应形成的CuSO4溶液显蓝色,而与盐酸反应形成的CuCl2溶液显绿色.
【提出问题】同样都含有Cu2+,为什么试管E中的CuSO4溶液显蓝色,而试管F中的CuCl2溶液显绿色.
【猜想与假设】
猜想一:若溶液中Cu2+显蓝色SO42-对Cu2+显色无影响,而Cl-对Cu2+显色有影响;
猜想二:若溶液中Cu2+显绿色,则SO42-对Cu2+显色有影响,而Cl-对Cu2+显色无影响;
猜想三:…
【实验验证】同学们用下列两种不同方案初步验证猜想一,请你补全实验所需试剂:
方案一:取少量试管E中的CuSO4溶液于另一支试管中,向其中加入足量适量的氯化钡溶液,观察到产生白色沉淀,溶液仍为蓝色的现象,猜想一正确.
方案二:取少量试管F中的CuCl2溶液于另一支试管中,向其中加入足量适量的硝酸银溶液,观察到产生白色沉淀,溶液由绿色变为蓝色的现象,猜想一正确.
【评价与反思】同学们在实验探究的过程中,体会到了溶液颜色成因复杂,相关知识还有待进一步学习.
实 验 内 容 |  |  |  |
| 实 验 现 象 | B(填字母编号) 瓶口的蓝色石蕊试纸很快变 红. | 两试管中均产生 气体 | 试管E:绿色粉末逐渐溶解,产生气泡,溶液显蓝色. 试管F:绿色粉末逐渐溶解,产生气泡,溶液显绿色. |
| 分 析 与 结 论 | 该酸有挥发性,另一种酸没有.不同的酸可能有不同的物理性质 | 不同的酸具有相似的化学性质,这是因为酸溶液中都含有H+(填符号). | 试管E中发生反应的化学方程式:Cu2(OH)2CO3+2H2SO4═ 2CuSO4+3H2O+CO2↑ 试管F中发生反应的化学方程式:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑ |
【提出问题】同样都含有Cu2+,为什么试管E中的CuSO4溶液显蓝色,而试管F中的CuCl2溶液显绿色.
【猜想与假设】
猜想一:若溶液中Cu2+显蓝色SO42-对Cu2+显色无影响,而Cl-对Cu2+显色有影响;
猜想二:若溶液中Cu2+显绿色,则SO42-对Cu2+显色有影响,而Cl-对Cu2+显色无影响;
猜想三:…
【实验验证】同学们用下列两种不同方案初步验证猜想一,请你补全实验所需试剂:
方案一:取少量试管E中的CuSO4溶液于另一支试管中,向其中加入足量适量的氯化钡溶液,观察到产生白色沉淀,溶液仍为蓝色的现象,猜想一正确.
方案二:取少量试管F中的CuCl2溶液于另一支试管中,向其中加入足量适量的硝酸银溶液,观察到产生白色沉淀,溶液由绿色变为蓝色的现象,猜想一正确.
【评价与反思】同学们在实验探究的过程中,体会到了溶液颜色成因复杂,相关知识还有待进一步学习.
11.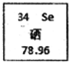 元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )
元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )
 元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )
元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )| A. | 是人体必需的微量元素 | B. | 原子核内质子数为34 | ||
| C. | 原子核内中子数为34 | D. | 相对原子质量为78.96 |
6.下列变化中,属于化学变化的是( )
| A. | 石蜡熔化 | B. | 汽油挥发 | C. | 湿衣晒干 | D. | 木材燃烧 |
 除去CO中的CO2
除去CO中的CO2 制取二氧化碳气体并收集
制取二氧化碳气体并收集 测定水的组成
测定水的组成
