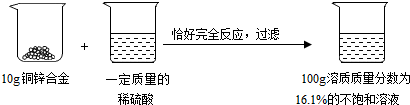
题目内容
4.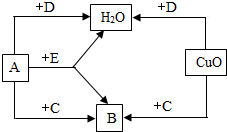 A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物,它们之间的转化关系如图所示.
A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物,它们之间的转化关系如图所示.(1)请写出你的推断结果:C一氧化碳,D氢气;
(2)请你写出下列转化的方程式:
①CuO与C反应生成BCO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
②A与E反应生成B和H2OCH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
分析 A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物,D能与氧化铜反应生成水,说明D具有还原性,D为氢气;A和氢气反应生成水,则A为氧气;C能与氧化铜反应,说明C也具有还原性,则C为一氧化碳,一氧化碳与氧化铜反应生成铜和二氧化碳,一氧化碳燃烧生成二氧化碳,则B为二氧化碳;E与氧气反应生成二氧化碳和水,则E为甲烷;据此进行分析解答.
解答 解:A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物,D能与氧化铜反应生成水,说明D具有还原性,D为氢气;A和氢气反应生成水,则A为氧气;C能与氧化铜反应,说明C也具有还原性,则C为一氧化碳,一氧化碳与氧化铜反应生成铜和二氧化碳,一氧化碳燃烧生成二氧化碳,则B为二氧化碳;E与氧气反应生成二氧化碳和水,则E为甲烷.
(1)C、D分别是一氧化碳、氢气.
(2)①CuO与C反应生成B,即一氧化碳与氧化铜反应生成铜和二氧化碳,反应的化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
②A与E反应生成B和H2O,即甲烷与氧气反应生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
故答案为:(1)一氧化碳;氢气;(2)①CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;②CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

 名校课堂系列答案
名校课堂系列答案| A. | CO和CO2的分子构成不同,所以化学性质不同 | |
| B. | 固体很难被压缩说明分子间有斥力 | |
| C. | 香气袭人说明分子在永不停息地运动 | |
| D. | 磁铁能吸引大头针说明分子间有引力 |
| A. | 酸能使紫色石蕊变红,CO2通入紫色石蕊溶液后溶液变红,所以CO2是酸 | |
| B. | 有机化合物都含有碳元素,因此所有含碳元素的化合物都是有机化合物 | |
| C. | 某物质可以导电,该物质一定是金属单质 | |
| D. | 常温下,测定某溶液的pH=5,该溶液一定呈酸性 |
| A. |  过滤液体 | B. |  收集H2 | C. |  实验室制取氧气 | D. |  测溶液pH |
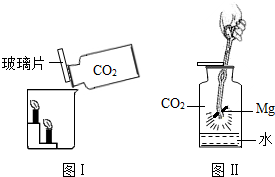 某兴趣小组在老师的带领下对“二氧化碳的化学性质”进行探究.
某兴趣小组在老师的带领下对“二氧化碳的化学性质”进行探究.(1)同学用如图Ⅰ所示装置对二氧化碳的灭火实验进行研究,他们观察到的现象是下面的蜡烛先熄灭,上面的蜡烛后熄灭;得出实验的结论是二氧化碳不支持燃烧,也不能燃烧;相同条件下,二氧化碳的密度比空气的大.
(2)老师又为同学们如图Ⅱ所示的兴趣实验,将打磨光亮的镁带在酒精灯上点燃,然后伸入到盛满二氧化碳的集气瓶中,冒出大量白烟,瓶壁并放出大量的热.
【提出问题】镁带在二氧化碳中燃烧的生成物是什么?
【查阅资料】①氧化镁、氢氧化镁均是白色难容于水的固体.
②MgO+2HCl=MgCl2+H2O.③MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
【猜想假设】
猜想一:黑色固体的成分是炭黑;猜想二:白烟的成分是氢氧化镁;你的猜想:白烟的成分是氧化镁;
同学们经过讨论认为猜想二不正确,他们推断的依据是反应中没有氢元素参加.
【实验探究】②为检验生成物的成分,做如下实验.
| 实验步骤 | 实验现象 | 实验结论和化学方程式 | |
| 向广口瓶中加入过量盐酸振荡,充分反应后过滤,在滤纸上留有黑色固体 | Ⅰ.将黑色固体收集.洗涤、干燥后,点燃,在火焰上方罩一个蘸有澄清石灰水的烧杯 | 黑色固体燃烧,烧杯内壁出现白色浑浊 | 猜想一正确,写出石灰水变浑浊反应的化学方程式是: CO2+Ca(OH)2=CaCO3↓+H2O. |
| Ⅱ.取少量滤液于试管中,逐滴加入氢氧化钠溶液 | 开始 无明显现象,后有白色沉淀产生 | 你的猜想正确 | |
【反思提高】实验室中由某些活泼金属引起的着火,不能用二氧化碳灭火,应用细沙灭火.