题目内容
18.如图表示某些物质间转化关系(“→”表示物质之间存在转化关系).其中A、B是由相同元素组成的无色液体,且A具有消毒杀菌作用;C、F为气体单质,F是空气中含量最高的气体;D、E为固体,D呈红棕色,E是应用最广泛的金属.G的相对分子质量为100,组成元素的原子个数比为3:2.回答下列问题: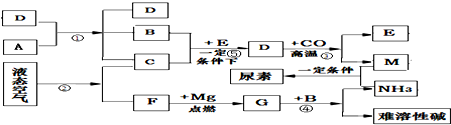
(1)①中C的化学式是O2;
(2)②处利用A不同(填序号,A.沸点 B.密度 C.溶解性),分离得两种气体;
(3)反应③④的化学方程式:③3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;④Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.
(4)在日常生活中为了避免反应⑤的发生可采取的措施是刷漆、涂油.
分析 根据A、B是由相同元素组成的无色液体,且A具有消毒杀菌作用,C、F为气体单质,A分解会生成B、C,所以A是过氧化氢溶液,B是水,C是氧气,D是二氧化锰,F是空气中含量最高的气体,所以F是氮气,E是应用最广泛的金属,所以E是铁,铁、氧气、水在一定条件下生锈,所以D是氧化铁,氧化铁和一氧化碳高温生成铁和二氧化碳,所以M是二氧化碳,氮气和镁在点燃的条件下生成氮化镁,所以G是氮化镁,氮化镁和水反应生成氢氧化镁和氨气,然后将推出的物质进行验证即可.
解答 解:A、B是由相同元素组成的无色液体,且A具有消毒杀菌作用,C、F为气体单质,A分解会生成B、C,所以A是过氧化氢溶液,B是水,C是氧气,D是二氧化锰,F是空气中含量最高的气体,所以F是氮气,E是应用最广泛的金属,所以E是铁,铁、氧气、水在一定条件下生锈,所以D是氧化铁,氧化铁和一氧化碳高温生成铁和二氧化碳,所以M是二氧化碳,氮气和镁在点燃的条件下生成氮化镁,所以G是氮化镁,氮化镁和水反应生成氢氧化镁和氨气,经过验证,推导正确;
(1)①中C是氧气,故填:O2;
(2)②处分离液态空气得到氮气和氧气,是利用沸点不同,故填:A;
(3)③是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,④是氮化镁和水反应生成氢氧化镁沉淀和氨气,化学方程式为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;
(4)要避免铁生锈,可以在铁制品表面刷漆或是涂油,故填:刷漆、涂油.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案| A. | 分解反应都属于氧化还原反应 | |
| B. | 置换反应都属于氧化还原反应 | |
| C. | 复分解反应都不属于氧化还原反应 | |
| D. | 有单质参加的化合反应属于氧化还原反应 |
| A. | 钢是很纯的铁 | |
| B. | 炼铁的主要设备为电炉 | |
| C. | 被腐蚀的铁制品属于不可回收垃圾 | |
| D. | 四氧化三铁中铁元素质量分数比氧化铁中的高 |
| A. | 氢氧化钠固体易潮解,有腐蚀性,称量时不能直接放在天平的托盘上 | |
| B. | 氧气可以支持燃烧,具有可燃性 | |
| C. | 经常用钢丝球洗刷铝锅,能使之光亮、耐用 | |
| D. | 钢铁闸门浸入水下的部分比靠近水面的部分更容易生锈 |
| A. | 水在固态时,水分子是静止不动的 | |
| B. | 保持水的化学性质的最小微粒是水分子 | |
| C. | 自来水厂的净水过程有:沉淀、过滤、吸附、消毒和煮沸 | |
| D. | 电解水的实验中,正负极产生的气体质量比为1:2 |
| A. | 用甲醛溶液浸泡海产品以保鲜 | |
| B. | 用汽油除去油污是利用了“乳化作用” | |
| C. | 燃烧法能够区分羊毛和涤纶 | |
| D. | 发现煤气泄漏时,应打开排风扇开关通风 |
 某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.
某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.探究活动一、金属镍和铜的活动性顺序
| 实验方案 | 实验现象 | 实验结论 |
| 将金属镍加入到盛有硫酸铜溶液的试管中 | 溶液的颜色变浅, 有红色固体析出 | 镍比铜的金属活动性强 |
实验过程中,小组同学还发现试管中有无色气体产生的“异常”现象,十分好奇,于是继续进行探究活动.
探究活动二、无色气体的成分是什么?
【猜想假设】A.氢气 B.氧气 C.二氧化硫 D.二氧化碳 E.一氧化碳
【分析推理】小明认为无色气体不可能是二氧化碳或一氧化碳,理由是反应前不含有碳元素.
小红根据二氧化硫能够形成酸雨的事实,推测二氧化硫与二氧化碳的化学性质相似.小组同学认为小红的观点合理,于是将收集到的气体通入石蕊溶液中,发现溶液不变色,证明无色气体不是二氧化硫.
综上所述,小组同学认为,无色气体可能是氢气,或者是氧气.
【设计方案】为确定气体成分,小组同学设计了如下实验方案:
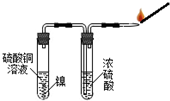
用图所示装置进行实验,先排一会气体,然后将燃着的木条放在尖嘴处,发现气体燃烧并发出淡蓝色火焰,证明无色气体可能是氢气.
该实验方案中浓硫酸的作用是吸水.
【评价与反思】小组同学认为,还可以补充一个实验,验证无色气体中含有氢元素,从而进一步证明无色气体可能是氢气.他们应补充的实验是在火焰上罩一个干而冷的烧杯,杯壁有水雾产生.
 生活中处处有化学,化学与生活密切相关.
生活中处处有化学,化学与生活密切相关.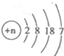 ,那么,溴原子核内质子数为35;溴原子易得到电子(填“得到”或“失去”).
,那么,溴原子核内质子数为35;溴原子易得到电子(填“得到”或“失去”).