题目内容
17.有A、B、C、D、E五种物质,它们之间有如下相互转化关系:①A+CuO→Cu+B ②B+H2O→C ③C$\stackrel{△}{→}$B+H2O④B+Ca(OH)2→D+H2O ⑤D$\stackrel{高温}{→}$B+金属氧化物
⑥B+A$\stackrel{高温}{→}$E
(1)试推断A.B.C.D.E各为什么物质(用化学式表示)
A.C B.CO2 C.H2CO3 D.CaCO3 E.CO
(2)写出①、④两个反应方程式,是氧化还原反应的注明还原剂:
①C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,C为还原剂 ④CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据A+CuO→Cu+B,可知A具有还原性,所以A可能是一氧化碳、碳或氢气,对应的B为二氧化碳或水;B+H2O→C,则B为二氧化碳,A不可能时氢气;③C$\stackrel{△}{→}$B+H2O,则C为碳酸,B+Ca(OH)2→D+H2O,则D为碳酸钙;根据B+A$\stackrel{高温}{→}$E,则A为碳,生成的E为一氧化碳,然后将推出的物质进行验证即可.
解答 解:(1)根据(1)A能与氧化铜反应生成铜和B,可知A具有还原性,则A可能是一氧化碳、碳或氢气,对应的B为二氧化碳或水,根据(2)C能分解为B和水,则B为二氧化碳,A不可能时氢气,根据(3)则C为碳酸,根据(4)二氧化碳能与氢氧化钙反应生成碳酸钙,则D为碳酸钙,根据(6)二氧化碳能与A反应生成E,则A为碳,生成的E为一氧化碳,经过验证,推导正确,所以A是C,B是CO2,C是H2CO3,D是CaCO3,E是CO;
(2)反应①是碳和氧化铜在高温的条件下反应生成铜和二氧化碳,化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,C为还原剂;
反应④是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:(1)C,CO2,H2CO3,CaCO3,CO;
(2)C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,C为还原剂;
CO2+Ca(OH)2=CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
12.向下列各组物质的混合溶液中滴加NaOH溶液,其现象与图象描述一致的是( )
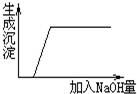

| A. | HCl和Ba(NO3)2 | B. | CuSO4和H2SO4 | C. | CuSO4和Na2SO4 | D. | Na2SO4和Ba(NO3)2 |
2.为减少温室气体排放,人们积极寻找不含碳元素的燃料.经研究,发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景.化学方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6x+2N2,生成物x为常见物质,关于物质x,下列说法正确的是( )
| A. | 该物质由氮、氢、氧三种元素组成 | B. | 该物质的化学式为H2O2 | ||
| C. | 该物质中氢元素的质量分数为7% | D. | 该物质中氢、氧元素的质量比为1:8 |
10.下列说法中,正确的是( )
| A. | 人体补充钙元素可预防贫血 | |
| B. | 鉴别羊毛和合成纤维可灼烧闻气味 | |
| C. | 治疗胃酸过多可服用氢氧化钠 | |
| D. | 提高农作物产量可将硝酸铵与熟石灰混合施用 |
11.下列实验方案的设计中,不正确的是( )
| A. | 用燃烧木炭的方法制备纯净的二氧化碳 | |
| B. | 用适量稀硫酸清除铁制品表面的铁锈 | |
| C. | 用紫色的石蕊溶液区分一氧化碳和二氧化碳 | |
| D. | 用足量稀盐酸检验久置的氢氧化钠固体是否变质 |

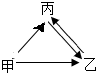 甲、乙、丙是三种初中化学常见的物质,相互转化关系如图所示,请完成下列问题:
甲、乙、丙是三种初中化学常见的物质,相互转化关系如图所示,请完成下列问题: