题目内容
15.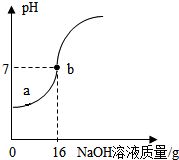 实验室欲测定一瓶标签破损的稀硫酸的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试回答:
实验室欲测定一瓶标签破损的稀硫酸的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试回答:(1)当pH=7时,消耗NaOH溶液中溶质的质量为0.8g.
(2)计算稀硫酸的溶质质量分数.
分析 (1)根据溶质质量分数的计算公式计算;
(2)根据稀H2SO4与NaOH溶液的反应的方程式,由NaOH的质量求出稀H2SO4的溶质稀H2SO4的溶质质量分数,
再求出稀H2SO4的溶质质量分数
解答 解:(1)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;
(2)10g稀硫酸样品含有H2SO4的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
0.8g x
$\frac{80}{0.8g}$=$\frac{98}{x}$
解得:x=0.98g
稀H2SO4的溶质质量分数为:$\frac{0.98g}{10g}$×100%=9.8%
故答案为:(1)0.8;(2)稀H2SO4的溶质质量分数是9.8%.
点评 此题是一道结合图象的计算题,解题时找到PH=7的恰好反应点,并利用化学方程式的计算进行解决是解题的突破口.

练习册系列答案
相关题目
5.下列有关物质燃烧现象的叙述中,正确的是( )
| A. | 铁丝在氧气中燃烧:火星四射,生成一种红色固体 | |
| B. | 镁条在空气中燃烧:发出耀眼的白光,只生成一种黑色固体 | |
| C. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 | |
| D. | 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体 |
6.能源和环境是人类生存的基本条件,下列叙述错误的是( )
| A. | 发展氢能是开发清洁能源 | B. | 过量排放CO2会形成酸雨 | ||
| C. | 石油是一种不可再生能源 | D. | 禁止焚烧秸秆 |
20.质量为Xg的碳与Yg的氧气在一密闭容器内充分反应得到(X+Y)g的气体,则碳与氧气的质量不可能为( )
| A. | 6g、16g | B. | 6g、6g | C. | 6g、10g | D. | 6g、8g |
7.2011年5月1日开始,《刑法修正案》和修改后的《道路交通安全法》开始实施,对醉酒驾车者一律刑事拘留,下表是国家对“饮酒驾车”和“醉酒驾车”的界定标准:
(1)某司机驾车时经交警检查每100毫升血液中酒精含量为126毫克,他属于醉酒驾车;
(2)乙醇(C2H5OH)俗名酒精,由3种元素组成,其中碳元素的质量分数为:52.2%.
| 饮酒驾车 | 20毫克/100毫升≤血液中的酒精含量<80毫克/100毫升 |
| 醉酒驾车 | 血液中的酒精含量≥80毫克/100毫升 |
(2)乙醇(C2H5OH)俗名酒精,由3种元素组成,其中碳元素的质量分数为:52.2%.