题目内容
8. 许多化学反应都伴随着明显的现象.但也有一些观察不到明显现象.某化学小组的同学探究二氧化碳与氢氧化钠反应的现象,设计了如下实验方案,请根据要求回答下列问题:
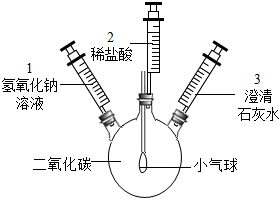
许多化学反应都伴随着明显的现象.但也有一些观察不到明显现象.某化学小组的同学探究二氧化碳与氢氧化钠反应的现象,设计了如下实验方案,请根据要求回答下列问题:(1)步骤一:如图所示,先将注射器1中的氢氧化钠溶液推入充满二氧化碳的瓶中,发现小气球鼓起,发生该现象的原因是NaOH溶液吸收CO2装置内压强变小,气球鼓起,发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
(2)步骤二:把注射器3在活塞向外拉,发现无明显现象.说明步骤1中装置内的CO2已被完全吸收.
(3)步骤三:将注射器2中的稀盐酸推入瓶中,发现溶液中有气泡产生,气球变瘪.发生反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(4)步骤四:把注射器3在活塞向外拉,发现澄清石灰水变浑浊.发生反应的化学方程式为Ca(OH)2+CO2═H2O+CaCO3↓.
由以上实验,该小组得出结论:二氧化碳能与氢氧化钠反应.
分析 (1)根据氢氧化钠与二氧化碳反应,使瓶内气压减小考虑;
(2)向外拉注射器3,根据现象可以检验二氧化碳的存在;
(3)根据盐酸能够和碳酸钠反应产生氯化钠、水和二氧化碳写出反应的方程式;
(4)根据二氧化碳和氢氧化钙反应产生碳酸钙沉淀和水写出反应的方程式.
解答 解:(1)NaOH溶液吸收CO2装置内压强变小,在外界大气压的作用下气球鼓起;二氧化碳和氢氧化钠反应产生碳酸钠和水;故填:NaOH溶液吸收CO2装置内压强变小,气球鼓起;2NaOH+CO2=Na2CO3+H2O;
(2)向外拉注射器3(或充分振荡),如果无任何现象,证明步骤1中装置内的CO2已被完全吸收;故填:步骤1中装置内的CO2已被完全吸收;
(3)盐酸能够和碳酸钠反应产生氯化钠、水和二氧化碳;故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(4)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故化学方程式是:Ca(OH)2+CO2═H2O+CaCO3↓.
点评 解答本题关键是要知道氢氧化钠与二氧化碳反应后,使瓶内压强减小,熟悉方程式的书写方法.

练习册系列答案
相关题目
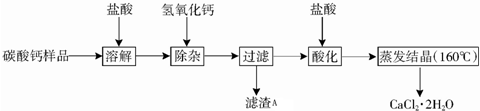
16.医用CaCl2•2H2O可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用CaCl2•2H2O的工艺流程为:
已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
(1)在实验室进行溶解时玻璃棒的作用是搅拌,加速溶解,过滤时用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是4.0~7.8;滤渣A的主要成分的化学式为Fe(OH)3、Al(OH)3.
(3)酸化时加盐酸的主要目的为了将氢氧化钙转化为氯化钙.
(4)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少?(写出计算过程)

已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.0 | 7.8 |
| 完全沉淀时的pH | 3.7 | 5.2 | 10.8 |
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是4.0~7.8;滤渣A的主要成分的化学式为Fe(OH)3、Al(OH)3.
(3)酸化时加盐酸的主要目的为了将氢氧化钙转化为氯化钙.
(4)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少?(写出计算过程)
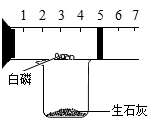 某同学用如图装置粗略地测定空气中氧气的体积分数,图中烧杯中盛放的生石灰(即氧化钙)与水反应生成氢氧化钙,同时放出大量热.烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内封有空气,活塞右端的玻璃管口跟外界空气连通.白磷很易燃且燃烧产物与红磷燃烧的产物相同,实验开始前活塞处在刻度5cm处.
某同学用如图装置粗略地测定空气中氧气的体积分数,图中烧杯中盛放的生石灰(即氧化钙)与水反应生成氢氧化钙,同时放出大量热.烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内封有空气,活塞右端的玻璃管口跟外界空气连通.白磷很易燃且燃烧产物与红磷燃烧的产物相同,实验开始前活塞处在刻度5cm处.


 小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):
小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):