题目内容
用金属铁制备自来水的新型消毒、净水剂K2FeO4的流程如下:
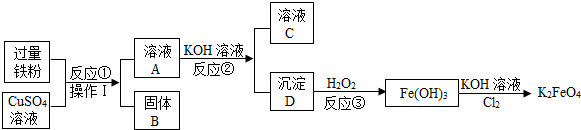
请回答下列问题:
(1)反应①的化学方程式为 ,固体B的成分是 ;
(2)操作I的名称是 ;
(3)A与KOH溶液发生复分解反应生成D,反应③是D 和H202发生化合反应,请写出反应③的化学方程式: .

请回答下列问题:
(1)反应①的化学方程式为
(2)操作I的名称是
(3)A与KOH溶液发生复分解反应生成D,反应③是D 和H202发生化合反应,请写出反应③的化学方程式:
考点:物质的相互转化和制备,金属的化学性质,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)根据反应①过量铁粉与硫酸铜的反应分析固体B的成分并书写化学方程式;
(2)根据过滤的原理分析回答;
(3)根据发生的反应写出反应的方程式.
(2)根据过滤的原理分析回答;
(3)根据发生的反应写出反应的方程式.
解答:解:(1)由反应的流程可知,过量的铁粉与硫酸铜反应,生成了硫酸亚铁和铜,由于铁是过量的,因此,在过滤后得到的固体B是Cu,Fe的混合物;化学方程式为:Fe+CuSO4═FeSO4+Cu;
(2)由上述反应①得到是固液的混合物,要将固液分开,应进行的操作是过滤;
(3)反应③是氢氧化亚铁被过氧化氢氧化为氢氧化铁,方程式是:2Fe(OH)2+H2O2=2Fe(OH)3
故答案为:(1)Fe+CuSO4═FeSO4+Cu;Cu,Fe;
(2)过滤;
(3)2Fe(OH)2+H2O2=2Fe(OH)3
(2)由上述反应①得到是固液的混合物,要将固液分开,应进行的操作是过滤;
(3)反应③是氢氧化亚铁被过氧化氢氧化为氢氧化铁,方程式是:2Fe(OH)2+H2O2=2Fe(OH)3
故答案为:(1)Fe+CuSO4═FeSO4+Cu;Cu,Fe;
(2)过滤;
(3)2Fe(OH)2+H2O2=2Fe(OH)3
点评:本题给出了制取物质的反应流程图,对于这类题目,需要搞清楚每一步反应物、生成物,清楚工艺流程原理.再结合有关的知识分析解答有关的问题.

练习册系列答案
相关题目
利用化学知识对下列说法进行判断,其中正确的是( )
| A、咀嚼米饭时会出现甜味,这一过程属于物理变化 |
| B、绿色植物合成葡萄糖的过程中将太阳能转化为化学能 |
| C、要提高澄清石灰水的溶质质量分数,可以升高该溶液的温度 |
| D、向鸡蛋清中加入饱和硫酸铵溶液出现白色沉淀,鸡蛋清中蛋白质失去了原有的生理功能 |






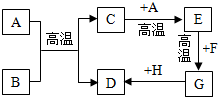 如图中A-H都是化学中常见的物质,已知A、B都是黑色固体,D、F为红色固体,G是目前年产量最高的金属.它们之间的转化关系如图所示.请推断出各物质后回答下列问题:
如图中A-H都是化学中常见的物质,已知A、B都是黑色固体,D、F为红色固体,G是目前年产量最高的金属.它们之间的转化关系如图所示.请推断出各物质后回答下列问题: