题目内容
6.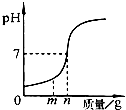 用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,往所得溶液中滴加紫色石蕊溶液,溶液呈红色.
用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,往所得溶液中滴加紫色石蕊溶液,溶液呈红色.
分析 熟石灰与盐酸反应生成氯化钙与水,写出反应的化学方程式即可.根据图象中pH值的变化是从小于7逐渐的增大到大于7,当加入溶液的质量为mg时,溶液的pH小于7,据此进行分析解答.根据质量守恒定律可以书写化学方程式,根据化学方程式和图中情况可以进行相关方面的计算.
解答 解:氢氧化钙和盐酸反应能生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H20;故填:Ca(OH)2+2HCl=CaCl2+2H20;
当加入熟石灰mg时,盐酸有剩余,溶液中的溶质是盐酸中的氯化氢和反应生成的氯化钙.故填:CaCl2和HCl.
由Ca(OH)2+2HCl=CaCl2+2H20; NaOH+HCl═NaCl+H2O 可知,氢氧化钙和盐酸反应的质量比是74:73.氢氧化钠和盐酸反应的质量比是80:73.加入ng氢氧化钙恰好完全反应,溶液显中性.加入ng氢氧化钠不能把盐酸反应完,即盐酸过量,溶液显酸性,能使紫色的石蕊试液变红色.故填:红.
点评 本题难度不大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
相关题目
17. 一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
 一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )| A. | 生成氧化镁的质量为m2g | B. | 参加反应镁的质量为m1g | ||
| C. | 参加反应氧气的质量为:(m2-m1)g | D. | 参加反应镁与氧气的质量比为3:4 |
1.下列说法不正确的是( )
| A. | 将一瓶20℃时的饱和硝酸钾溶液倒出$\frac{1}{4}$后,剩余溶液仍然饱和 | |
| B. | 清新的空气是一种溶液 | |
| C. | 一定温度下的食盐饱和溶液还可以溶解氯化镁 | |
| D. | 某温度下的饱和溶液,升高温度都可以变成不饱和溶液 |
11.下列四种粒子的结构示意图中,最容易形成阳离子的是( )
| A. | 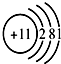 | B. | 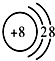 | C. | 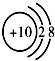 | D. | 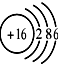 |
16.“催化转化器”可以将汽车尾气中有害气体处理为无污染的气体,如图为该反应的微观示意图,其中不同颜色的球代表不同的原子.下列说法正确的是( )
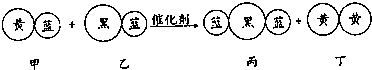
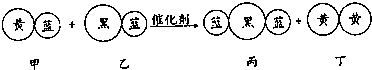
| A. | 乙和丙中所含的元素种类不同 | B. | 甲和丁中同种元素的化合价相等 | ||
| C. | 该反应中共有三种元素 | D. | 乙和丁都是化合物 |
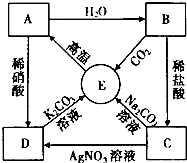 A~E均为初中化学常见物质,A、B、C、D、E均含有同一种元素,B常用于改良酸性土壤.它们之间的相互转化关系如图所示:(图中“→”表示物质间存在转化关系,部分生成物已略去).请回答下列问题:
A~E均为初中化学常见物质,A、B、C、D、E均含有同一种元素,B常用于改良酸性土壤.它们之间的相互转化关系如图所示:(图中“→”表示物质间存在转化关系,部分生成物已略去).请回答下列问题: