题目内容
16.某品牌可乐的配料中有水、白砂糖、二氧化碳、磷酸(H3PO4)、焦糖色、食用香精等.请用化学用语填写下列空白.1个磷酸分子中含有3个氢原子、1个磷原子和4O.该可乐中除磷酸外,还含有的一种酸是H2CO3.白砂糖的主要成分是蔗糖,1个蔗糖分子在人体中经氧化生成12个二氧化碳分子12CO2,同时为人体提供能量,打开汽水瓶盖,有大量气泡自动涌出,检验该气体的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O.
分析 1个磷酸分子中含有3个氢原子、1个磷原子和4个氧原子,原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
该可乐中除磷酸外,还含有的一种酸是碳酸.
分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字.
打开汽水瓶盖,有大量气泡自动涌出,该气体是二氧化碳,检验二氧化碳用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,进行分析解答.
解答 解:1个磷酸分子中含有3个氢原子、1个磷原子和4个氧原子,由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故4个氧原子表示为:4O.
该可乐中除磷酸外,还含有的一种酸是碳酸,其化学式为:H2CO3.
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则12个二氧化碳分子可表示为:12CO2.
打开汽水瓶盖,有大量气泡自动涌出,该气体是二氧化碳,检验二氧化碳用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:4O;H2CO3;12CO2;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、化学式、化学方程式等)的书写方法是正确解答此类题的关键.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
4.下列物质的用途与性质对应不正确的是( )
| 物 质 | 用 途 | 性 质 | |
| A | 氢氧化钠固体 | 作某些气体的干燥剂 | 氢氧化钠固体具有吸水性 |
| B | 熟石灰 | 改良酸性土壤 | 熟石灰能与酸发生中和反应 |
| C | 活性炭 | 净化水 | 活性炭具有吸附性 |
| D | 氧气 | 炼钢 | 氧气具有可燃性 |
| A. | A | B. | B | C. | C | D. | D |
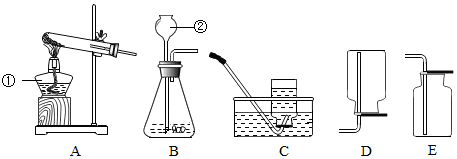
8.如图表示初中化学常见实验操作,其中正确的是( )
| A. |  | B. |  | C. |  | D. |  |