题目内容
10.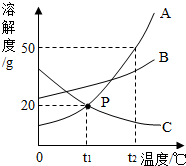 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答:(1)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液饱和(填“饱和”还是“不饱和”),溶液质量是60g,溶液的溶质质量分数是16.7%;
(2)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是B>A>C.
分析 (1)根据t1℃时A的溶解度为20g,进行分析解答.
(2)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,AB的溶解度增大,但溶液的组成为发生改变;C的溶解度减小,有C物质析出,据此进行分析解答.
解答 解:(1)t1℃时A的溶解度为20g,其涵义是t1℃时,100g水中最多溶解20gA,溶液达到饱和状态,则t1℃时30gA物质加入到50g水中不断搅拌,最多只能溶解10g,
形成的溶液是饱和溶液;形成溶液质量是10g+50g=60g;溶液的溶质质量分数是$\frac{10g}{60g}$×100%≈16.7%.
(2)t1℃时A、B、C三种物质的溶解度由大到小的顺序是B>C=A,t1℃时B饱和溶液中溶质质量分数最大;将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,AB的溶解度增大,但溶液的组成为发生改变,溶质的质量分数不变;C的溶解度减小,有C物质析出,但t2℃时C的溶解度小于t1℃时A的溶解度,故t2℃时C的饱和溶液中溶质质量分数小于t1℃时A的溶质质量分数,故三种溶液的溶质分数由大到小关系是B>A>C.
故答案为:(1)饱和;60;16.7%;(2)B>A>C.
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度曲线的理解,培养学生灵活运用知识解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.在生产生活中,很多问题都涉及化学知识,下列认识不正确的是( )
| A. | 工业“三废”和生活污水处理后再排放 | |
| B. | 为使农作物高产,大量施用化肥和农药 | |
| C. | 太阳能热水器既节能又环保 | |
| D. | 二氧化硫,二氧化氮,一氧化碳都是大气污染物 |
18.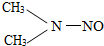 复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )
复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )
 复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )
复旦大学投毒案中用的N-亚硝基二甲胺,又称二甲基亚硝胺,是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品,具有强肝脏毒性,对人类很可能有致癌性.主要用于火箭燃料、抗氧剂等制造.其结构如图,对其认识错误的是( )| A. | 该物质由四种元素组成 | B. | 该物质具有易燃性 | ||
| C. | 该物质应该密封保存 | D. | 该物质燃烧的产物中有氮气 |
5.区分下列各组物质的两种方法都正确的是( )
| 需区分物质 | 方法一 | 方法二 | |
| A | 铁粉和氧化铜 | 观察颜色 | 加入稀硫酸观察现象 |
| B | 硝酸铵和硫酸钾固体 | 加氢氧化钙研磨 | 加入适量水观察是否溶解 |
| C | 羊毛制品和纯棉制品 | 点燃闻气味 | 观察颜色 |
| D | 稀盐酸和氢氧化钠溶液 | 加入大理石 | 加入硫酸铜溶液 |
| A. | A | B. | B | C. | C | D. | D |
15.鉴别日常生活中的下列各组物质,操作1和操作2均有错误的是( )
| 选项 | 鉴别的物质 | 操作1 | 操作2 |
| A | 软水和硬水 | 滴加肥皂水 | 加热蒸发 |
| B | 氯化钠和氢氧化钠 | 滴加盐酸 | 通入二氧化碳 |
| C | 氧气和二氧化碳 | 滴加紫色石蕊试液 | 伸入燃着的木条 |
| D | 真黄金和假黄金(铜锌合金) | 滴加稀盐酸 | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |
2.成语被誉为中华民族的瑰宝.下列成语中,其本意主要是化学变化的是( )
| A. | 花香四溢 | B. | 海市蜃楼 | C. | 蜡炬成灰 | D. | 木已成舟 |
19.下列图象不能正确反映其对应操作的是( )
| A. |  常温下向PH=10的NaOH溶液加稀盐酸 | |
| B. | 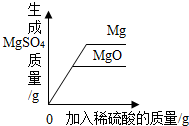 向等质量的Mg和MgO中分别加入足量等浓度的稀硫酸 | |
| C. | 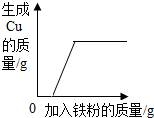 向一定量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉 | |
| D. | 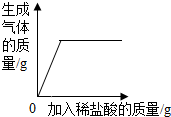 向一定量的部分变质的氢氧化钠溶液中滴加足量的稀盐酸 |
20.分别将下列各组中的三种物质的溶液混合,且其中的酸过量,最终有沉淀生成的一组是( )
| A. | NaOH FeCl3 HCl | B. | NaOH CuSO4 H2SO4 | ||
| C. | K2CO3 HCl Ba(OH)2 | D. | BaCl2 Na2SO4 HNO3 |