题目内容
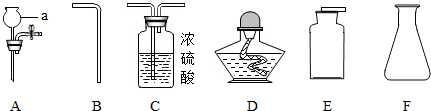
2.金属在生产和生活中有广泛的应用.(1)下列铜制品中,利用金属导热性的是C (填字母序号).

(2)铁制品在空气中易锈蚀,其实质是铁与空气中的氧气、水等接触后发生化学反应.
(3)已知金属M和N能够发生如下反应:M+H2SO4═MSO4+H2↑ Fe+MCl2═M+FeCl2 N+FeCl2═Fe+NCl2,判断Fe、Cu、M、N的活动性由强到弱的顺序是N>Fe>M>Cu.
(4)某兴趣小组在实验室发现了一块绿色的孔雀石标本,查阅资料知其主要成分是Cu2(OH)2CO3.他们以Cu2(OH)2CO3原料制取铜,其工艺流程如图所示:
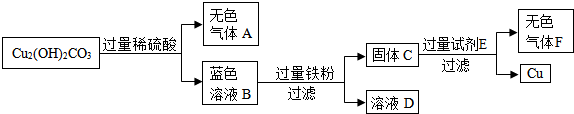
①过滤操作中用到的铁制仪器为铁架台.
②无色气体A的化学式是CO2,大气中该气体含量不断上升,会导致温室效应增强,全球气候变暖.
③写出蓝色溶液B与铁粉反应的化学方程式Fe+CuSO4=FeSO4+Cu.试剂E可选用稀硫酸溶液.
分析 (1)物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可;
(2)根据铁生锈的条件进行分析解答;
(3)根据金属活动性顺序的具体应用对金属的活动性进行分析,依据反应的反应物生成物种类判断反应的类型;
(4)根据碱式碳酸铜和过量的硫酸反应会生成硫酸铜、水和二氧化碳,所以蓝色溶液B是硫酸铜溶液,其中含有反应剩余的稀硫酸,硫酸铜和铁反应会生成硫酸亚铁和铜,所以C中含有铁和铜,溶液D中含有硫酸亚铁和硫酸,铁和硫酸反应生成硫酸亚铁和氢气,所以F是氢气,然后将推出的各物质代入转化关系中验证即可.
解答 解:(1)铜质奖牌是利用其金属光泽,铜导线是利用其导电性,铜火锅是利用其导热性,故填:C;
(2)铁在与水和氧气并存时易生锈,故填:水;
(3)由金属活动性顺序的具体应用可知:活动性在氢前的金属可以与稀酸反应生成氢气,金属活动性强的金属可以把金属活动性比它弱的金属从其盐溶液中置换出来,所以据M+H2SO4═MSO4+H2↑ Fe+MCl2═M+FeCl2 N+FeCl2═Fe+NCl2可知:M活动性在氢前且比铁弱,N活动性在比铁强,结合金属活动性顺序表可知四种金属的活动性顺序是:N>Fe>M>Cu,故填:N>Fe>M>Cu;
(4)碱式碳酸铜和过量的硫酸反应会生成硫酸铜、水和二氧化碳,所以蓝色溶液B是硫酸铜溶液,其中含有反应剩余的稀硫酸,硫酸铜和铁反应会生成硫酸亚铁和铜,所以C中含有铁和铜,溶液D中含有硫酸亚铁和硫酸,铁和硫酸反应生成硫酸亚铁和氢气,所以F是氢气,碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,硫酸铜和铁反应生成硫酸亚铁和铜,铁和硫酸反应生成硫酸亚铁和氢气,推导合理.
①过滤操作中用到的仪器有:烧杯、漏斗、玻璃棒、铁架台、滤纸等,所以过滤操作中用到的铁制仪器为:铁架台;
②通过推导可知A是二氧化碳,化学式为:CO2,大气中二氧化碳含量增多,会导致温室效应增强,全球气候变暖,故填:CO2; 温室效应;
③铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;通过推导可知固体C中含有铁和铜,铁排在氢之前,铜排在氢之后,所以试剂E可选用稀硫酸溶液.
故答案为:(1)C;
(2)水;
(3)N>Fe>M>Cu;
(4)①铁架台;
②CO2; 温室效应;
③Fe+CuSO4=FeSO4+Cu;稀硫酸.
点评 本题主要考查了金属的用途,完成此题,可以依据已有的金属的性质进行.

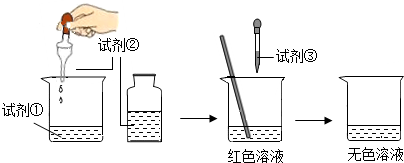
| A. | 稀NaOH溶液、石蕊溶液、稀盐酸 | B. | 稀盐酸、石蕊溶液、稀NaOH溶液 | ||
| C. | 稀NaOH溶液、酚酞溶液、稀盐酸 | D. | 稀盐酸、酚酞溶液、稀NaOH溶液 |
| A. | 钢铁冶炼 | B. | 石油分馏 | C. | 干冰升华 | D. | 海水晒盐 |
| A. | KMnO4、K2MnO4 | B. | P2O3、Ca2(PO4)2 | C. | NH4Cl、HNO3 | D. | Cl2、CaCl2 |
| A. | 滤液中一定存在Zn(NO3)2 | B. | 滤液中可能存在Ag+ | ||
| C. | 滤渣中一定含有单质Ag | D. | 滤渣中一定含有单质Cu |
| A. | 皂甙属于有机物 | B. | 一个皂甙分子中含有72个原子 | ||
| C. | 皂甙由三种元素组成 | D. | 皂甙中氢、氧元素质量为14:1 |