题目内容
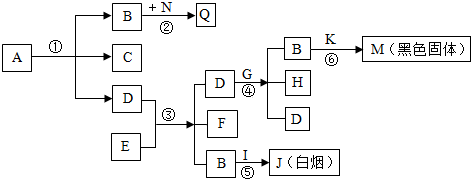
1.已知某固体混合物中可能含有CuO、BaCl2、Na2SO4、Na2CO3、CaCO3五种物质中的两种或多种.实验过程和出现的现象如图中所述:(设过程中所有发生的反应均恰好完全反应)
根据上述实验过程和发生的现象,请你回答下列问题:
(1)气体A的化学式为CO2.
(2)实验过程中反应②的化学方程式CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
(3)在滤液D中,肯定存在的阴离子是Cl-.(写离子符号)
(4)该固体混合物中,肯定存在的物质是BaCl2、CuO、Na2SO4.
分析 本题属于推断题,根据题目给出的流程图和信息:蓝色沉淀是氢氧化铜,因此原混合物中一定有氧化铜;依据含有的物质的情况以及加盐酸会生成气体,因故原混合物中Na2CO3、CaCO3至少有一种;因为加入盐酸后白色沉淀C不溶,因此C是硫酸钡,那么原混合物中一定有BaCl2和Na2SO4.
解答 解:解:根据题目给出的流程图和信息:蓝色沉淀是氢氧化铜,因此原混合物中一定有氧化铜;依据含有的物质的情况以及加盐酸会生成气体,故原混合物中Na2CO3、CaCO3至少有一种;因为加入盐酸后白色沉淀C不溶,因此C是硫酸钡,那么原混合物中一定有BaCl2和Na2SO4;
(1)由初中学过的知识可知,含有的物质的情况以及加盐酸会生成气体,则该气体只能是二氧化碳;
(2)实验②时滤液B与氢氧化钠的反应,B中含有氧化铜和盐酸的反应的产物,所以该反应是氯化铜和氢氧化钠的反应,化学方程式为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl;
(3)因为加入了盐酸,因此在滤液C中,肯定存在的阴离子是氯离子(Cl-);
(4)蓝色沉淀是氢氧化铜,因此原混合物中一定有氧化铜,依据含有的物质的情况以及加盐酸会生成气体,因此原混合物中Na2CO3、CaCO3至少有一种;因为加入盐酸后白色沉淀C不溶,因此E是硫酸钡,那么原混合物中一定有BaCl2和Na2SO4;故答案为:BaCl2、CuO、Na2SO4.
故答案为:(1)CO2;
(2)CuCl2+2NaOH=Cu(OH)2↓+2NaCl;
(3)Cl-;
(4)BaCl2、CuO、Na2SO4.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
11.下列物质露置于空气中,因发生化学反应而使质量增加的是( )
| A. | 浓硫酸 | B. | 烧碱溶液 | C. | 浓盐酸 | D. | 食盐溶液 |
9.下列叙述或操作正确的是( )
| A. | 长期饮用纯净水有益身体健康 | |
| B. | 将pH试纸伸入待测液中,等pH试纸变色后与标准比色卡比较,测出待测液的pH值 | |
| C. | 当入射光线与反射光线的夹角为60°时,反射角为30° | |
| D. | 镜面反射遵守光的反射规律,漫反射不遵守光的反射规律 |
16.近日,有媒体报道称:国内某知名品牌饮用水被指产品标准还不如自来水.下表为我国生活饮用水国家标准的部分内容,请回答下列问题.
(1)测得某地区合格饮用水的pH=6.6,可知该水略呈酸性(填“酸”或“碱”),通常是因为水中有一种常见弱酸是H2CO3(填化学式).
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子可表示为3Al3+.
(3)水的硬度较大时,煮沸后饮用是降低硬度的好办法,其化学原理是水中的Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.
生活饮用水水质常规检验项目及限值(部分)
因而水垢的主要成分有2种,请写出醋酸(用HAc代表醋酸)与水垢中碳酸钙反应的化学方程式CaCO3+2HAc=Ca(Ac)2+H2O+CO2↑.
(4)1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过180mg.
(1)测得某地区合格饮用水的pH=6.6,可知该水略呈酸性(填“酸”或“碱”),通常是因为水中有一种常见弱酸是H2CO3(填化学式).
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子可表示为3Al3+.
(3)水的硬度较大时,煮沸后饮用是降低硬度的好办法,其化学原理是水中的Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.
生活饮用水水质常规检验项目及限值(部分)
| 项 目 | 限 值 |
| 色度 浑浊度 pH 总硬度(以CaCO3计) 铝 铁 硫酸盐 | 不超过15度,并不得呈现其他异色 不超过1度,特殊情况下不超过5度 6.5-8.5 450mg/L 0.2mg/L 0.3mg/L 250mg/L |
(4)1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过180mg.
11.下列现象或事实,用粒子的相关知识加以解释,其中正确的是( )
| 现象或事实 | 解释 | |
| A | 夏天钢轨之间的缝隙变小 | 原子的体积热胀冷缩 |
| B | 氯化钠固体溶解于水不见了 | 氯化钠分子运动到水分子中间去了 |
| C | 氧气可供人呼吸,一氧化碳有毒 | 构成物质的分子不同,物理性质不同 |
| D | 在溶液中进行的化学反应速率快 | 溶液中的离子或分子间接触几率较大 |
| A. | A | B. | B | C. | C | D. | D |

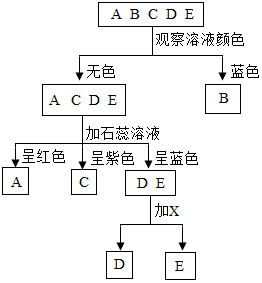 现有A、B、C、D、E五种溶液,它们分别是氢氧化钠溶液、硫酸铜溶液、碳酸钠溶液、氯化钠溶液和稀硫酸中的一种.鉴别它们可按下图所示的步骤进行.
现有A、B、C、D、E五种溶液,它们分别是氢氧化钠溶液、硫酸铜溶液、碳酸钠溶液、氯化钠溶液和稀硫酸中的一种.鉴别它们可按下图所示的步骤进行.