题目内容
1.下列叙述正确的是( )| A. | 打开浓盐酸的试剂瓶盖,瓶口出现白烟 | |
| B. | 用浓硫酸在白纸上写字,白纸上的字迹慢慢变黑 | |
| C. | 把鼻孔凑到容器口闻气体的气味 | |
| D. | 稀硫酸沾到皮肤或衣服上,处理无需处理 |
分析 A、根据浓盐酸具有挥发性,进行分析判断.
B、根据浓硫酸具有强腐蚀性进行分析判断.
C、根据闻气味的方法分析解答;
D、根据稀硫酸也具有腐蚀性进行分析判断
解答 解:A、浓盐酸具有挥发性,打开浓盐酸的试剂瓶盖,瓶口有白雾产生,不是烟;故选项说法错误.
B、浓硫酸具有强腐蚀性,浓硫酸在白纸上写字,白纸上的字迹慢慢变黑,故选项说法正确.
C、不能把鼻孔凑到容器口闻气体的气味,而是用用手扇动,让气体飘入鼻孔,故选项说法错误.
D、稀硫酸也具有腐蚀性,所以稀硫酸沾到皮肤或衣服上,也应该及时处理,故选项说法错误.
故选:B.
点评 本题难度不大,掌握酸的化学性质、浓盐酸具有挥发性即可正确解答本题.

练习册系列答案
相关题目
9.下列物质中,按单质、化合物、混合物顺序排列的是( )
| A. | 二氧化碳、水、空气 | B. | 氢气、海水、可口可乐 | ||
| C. | 氧化镁、矿泉水、食盐 | D. | 汞、冰、生理盐水 |
13.甲同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬的.她想到在学过的金属活动性顺序中并没有金属铬,为比较铬与常见金属铁、铜的活动性强弱,她和同学们在应用所学知识进行分析的基础上,提出了以下猜想,并进行了实验探究.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】
铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)
【甲同学实验】
甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
【乙同学实验】
乙同学为验证甲同学的结论,又设计了以下实验.
【实验反思】
(1)你认为乙同学没有必要做的实验是试管5中的实验没有必要做.
(2)请你结合所给的实验药品再设计一个实验,验证甲同学的结论.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】
铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)
【甲同学实验】
甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管1 | 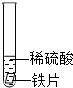 | 铁片表面产生气泡较慢,溶液变为浅绿色. | (1)实验前用砂纸打磨金属片的目的是 除去金属表面的氧化膜. (2)甲同学得到的结论是猜想1正确,他得到此结论的依据是 试管1中实验现象铁片表面产生气泡较慢,溶液变为浅绿色,可知金属铁在金属活动顺序中排在氢前,根据铬片表面产生气泡较快,溶液变为蓝色,从而得出铬也排在氢前且铬比铁活泼,因为铜不能和稀硫酸反应生成氢气. |
| 试管2 | 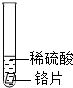 | 铬片表面产生气泡较快,溶液变为蓝色. | |
| 试管3 | 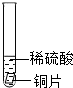 | 铜片上没有变化. |
乙同学为验证甲同学的结论,又设计了以下实验.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管4 | 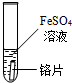 | \ | (1)甲同学的结论正确. (2)请写出铬与硫酸铜反应的化学方程式 Cr+CuSO4=CuSO4+Cr. |
| 试管5 | 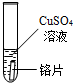 |
(1)你认为乙同学没有必要做的实验是试管5中的实验没有必要做.
(2)请你结合所给的实验药品再设计一个实验,验证甲同学的结论.
| 实验操作 | 实验现象 | 结论与解释 |
在试管中放入打磨光亮的铁片,再加入CrSO4溶液 | 铁片没有变化 | 甲同学的结论正确. |
10.X元素原子的核电荷数为n,X2-离子和Y3+离子的电子层结构相同,则Y原子的质子数是( )
| A. | n+1 | B. | n+2 | C. | n+3 | D. | n+5 |

