题目内容
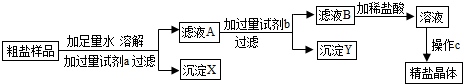
从蓝绿色硫酸铜溶液中提取金属铜、并制取硫酸亚铁.现利用该溶液制取金属铜,过程如下:

①操作2的名称为 ,加入过量的A的目是 ,固体M质量比最后得到的铜质量 ;
②加入足量B的目的是 .

①操作2的名称为
②加入足量B的目的是
考点:金属的化学性质,过滤的原理、方法及其应用
专题:金属与金属材料
分析:在金属活动性顺序中,只有排在氢前面的金属才可以和稀酸溶液反应生成氢气,只有活泼的金属才可以把排在它后面的金属从盐溶液中置换出来,因此为从蓝绿色溶液中提取金属铜,应该加入一种金属活动性比铜强的金属;从题意可知,由于加入的这种金属是过量,也就是我们得到的铜中混有这种过量的金属,而铜在氢后,不和稀酸溶液反应,因此加入的这种金属应该是排在氢前的金属.
解答:解:
①由于为从硫酸铜溶液中得到铜,应在溶液中加入一种排在氢前的金属,如:铁或锌等,加入金属后,完全反应后就得到了金属和新的溶液,为了把金属和溶液分开,因此应该采取过滤的方法.因为固体M为铜和过量的铁,所以固体M质量比最后得到的铜质量 多;
②由于加入的金属是过量的,为了把过量的金属铁或者是锌除去应该加入稀酸溶液,故答案为:完全除去过量的A.
故答案为:
①过滤,使溶液中的硫酸铜完全反应,多;②完全除去过量的A.
①由于为从硫酸铜溶液中得到铜,应在溶液中加入一种排在氢前的金属,如:铁或锌等,加入金属后,完全反应后就得到了金属和新的溶液,为了把金属和溶液分开,因此应该采取过滤的方法.因为固体M为铜和过量的铁,所以固体M质量比最后得到的铜质量 多;
②由于加入的金属是过量的,为了把过量的金属铁或者是锌除去应该加入稀酸溶液,故答案为:完全除去过量的A.
故答案为:
①过滤,使溶液中的硫酸铜完全反应,多;②完全除去过量的A.
点评:本题难度较大,主要考查了金属的有关的化学性质,培养学生分析问题、解决问题的能力.

练习册系列答案
相关题目
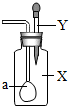 如图所示、广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入广口瓶中,振荡,一段时间后可见小气球a膨胀鼓起.下表中的各组物质不会出现上述现象的是( )
如图所示、广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入广口瓶中,振荡,一段时间后可见小气球a膨胀鼓起.下表中的各组物质不会出现上述现象的是( )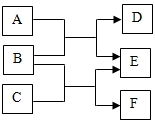 A--F是初中化学中的常见物质,它们有如图所示的转化关系,试回答下列问题:
A--F是初中化学中的常见物质,它们有如图所示的转化关系,试回答下列问题: