题目内容
16.元素周期表是化学学习的重要工具,依据下表回答问题: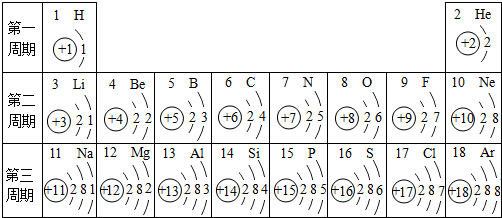
(1)表中13号元素属于金属(填“金属”或“非金属”)元素,在化学反应中易失去(填“失去”或“得到”)电子,形成Al3+(填离子符号).
(2)氟化钠的化学式为NaCl.
(3)H、Li、Na三种金属元素的原子失电子能力逐渐增强,我能根据这三种金属元素的原子结构推测:金属元素的原子失电子能力的强弱主要与最外层电子数、电子层数有关.
分析 (1)原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子;
(2)根据化合物的化学式的写法来分析;
(3)根据原子结构示意图分析解答.
解答 解:(1)表中13号元素的原子最外层电子数为3,小于4,是铝元素,属于金属元素,在化学反应中易失去3个电子而形成阳离子;故填:金属;失去;Al3+;
(2)钠原子最外层有一个电子,在化学变化中易失去一个电子而显+1价,氯原子最外层有7个电子,在化学变化中易得到一个电子而显-1价,故其化学式为NaCl;故填:NaCl;
(3)钾原子有4个电子层,最外层电子为1,钠原子和镁原子有3个电子层,钠原子最外层有1个电子,镁最外层有两个电子,所以金属单质失电子能力的强弱 与最外层电子数或电子层数有关.故填:最外层电子数;电子层数.
点评 明确元素周期表的排列原则及特点,了解原子结构示意图是解答本题关健.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
7.锰(Mn)和镍(Ni)都是金属,将镍丝插入硫酸锰溶液中,无变化;将镍丝插入硫酸铜溶液中,镍丝上铜析出.则Mn、Ni、Cu的金属活动性由强到弱排列正确的是( )
| A. | Mn Cu Ni | B. | Cu Ni Mn | C. | Ni Mn Cu | D. | Mn Ni Cu |
11.把锌粉放入硝酸银、硝酸铜和硝酸镁的混合溶液中,充分反应后过滤,所得固体中一定没有的是( )
| A. | 锌 | B. | 镁 | C. | 铜 | D. | 银 |
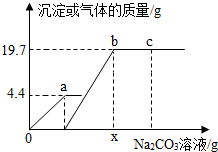 向一定质量BaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.请回答:
向一定质量BaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.请回答: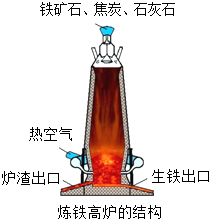 钢铁是人类生产生活中应用最广泛的金属材料,如图是炼铁高炉的结构示意图,请回答下列与此有关的问题:
钢铁是人类生产生活中应用最广泛的金属材料,如图是炼铁高炉的结构示意图,请回答下列与此有关的问题: