题目内容
2.某厂烟气中SO2的平均含量为0.04g/L,用780g硫化钠(Na2S)溶液恰好能吸收2000L该厂烟气中的SO2,反应的化学方程式为:2Na2S+5SO2+2H2O═4NaHSO3+3S↓.计算:
(1)生成硫的质量.
(2)理论上得到NaHSO3溶液的质量(假设烟气中其他成分不能被吸收).
分析 根据化学方程式有二氧化硫可计算出生成硫的质量,再根据质量守恒定律即可解答;
解答 解:2000L该厂烟气中的SO2的质量:2000L×0.04g/L=80g,
设生成S的质量为x,
2Na2S+5SO2+2H2O═4NaHSO3+3S↓
320 96
80g x
$\frac{320}{80g}=\frac{96}{x}$
x=24g
溶液质量:80g+780g-24g=836g.
答:
(1)生成硫的质量为24g
(2)得到 NaHSO3 溶液的质量为836g.
点评 本题主要考查根据化学方程式的计算以及结合质量守恒定律来解答,要学会巧用质量守恒定律.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
13.物质的用途与性质密切相关,下列说法合理的是( )
| A. | 无水硫酸铜用于检验水份的存在 | |
| B. | 碱石灰用于干燥CO2气体 | |
| C. | Ca(OH)2可用于治疗缺钙症 | |
| D. | NaOH溶液能吸收污染空气的有害气体NO2、SO2和CO |
17.某化学兴趣小组进行了复分解反应发生条件的探究实验.
(1)氢氧化钠和硫酸铜溶液能发生反应,是因为有沉淀生成,符合复分解反应发生条件
(2)对盐酸和氢氧化钠反应后溶液中的溶质进行探究.
【做出猜测】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
猜想四:有HClNaOH
你认为猜想猜想四不合理,其理由是HCl和NaOH不能共存
【设计实验】
(3)粗盐水中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4等杂质,以下是将粗盐水进行提纯得到氯化钠的实验流程:
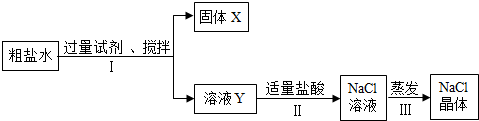
回答下列问题:
①固体X中含有的物质有硫酸钡、氢氧化镁和碳酸钙
②步骤I所加试剂中,不能用Ba(NO3)2代替BaCl2,其原因是什么?
(4)用氢氧化钠溶液中和一定量石油产品中的残余硫酸至中性,共消耗5%的氢氧化钠溶液80%,则此石油产品中含H2SO4的质量是多少?
(1)氢氧化钠和硫酸铜溶液能发生反应,是因为有沉淀生成,符合复分解反应发生条件
(2)对盐酸和氢氧化钠反应后溶液中的溶质进行探究.
【做出猜测】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
猜想四:有HClNaOH
你认为猜想猜想四不合理,其理由是HCl和NaOH不能共存
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入 少量的碳酸钠 | 有气泡生成 | 猜想三成立 |

回答下列问题:
①固体X中含有的物质有硫酸钡、氢氧化镁和碳酸钙
②步骤I所加试剂中,不能用Ba(NO3)2代替BaCl2,其原因是什么?
(4)用氢氧化钠溶液中和一定量石油产品中的残余硫酸至中性,共消耗5%的氢氧化钠溶液80%,则此石油产品中含H2SO4的质量是多少?
11.“群众利益无小事,食品安全是大事”.下列做法不会导致食品对人体产生危害的是( )
| A. | 在牛奶中添加三聚氰胺以增加含氮量 | |
| B. | 在麦片中加入少量乳酸亚铁以给人体补充铁元素 | |
| C. | 用甲醛水溶液浸泡水产品以达到杀菌和保鲜作用 | |
| D. | 用工业酒精勾兑食用酒以降低生产成本 |
12.关于化学反应A+B=C+D,下列说法不正确的是( )
| A. | 若A是可溶性碱,B是可溶性盐,则C和D可能是两种沉淀 | |
| B. | 若A和C是单质,B和D是化合物,则该反应一定是置换反应 | |
| C. | 若C和D分别是盐和水,则该反应物是中和反应 | |
| D. | 若A、B各取10g混合使其充分反应,则生成的C、D质量总和不一定是20g |
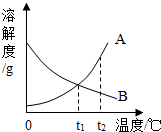 如图是A、B两种物质的溶解度曲线,根据图是回答下列问题:
如图是A、B两种物质的溶解度曲线,根据图是回答下列问题: