题目内容
15.某实验小组探究酸的化学性质,在做盐酸除铁锈的实验时发现:(1)将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(2)课后清洗仪器时,一同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为氯化亚铁溶液.这是由于过量的铁继续与黄色溶液的主要成分反应造成的,该反应的化学方程式为Fe+2FeCl3=3FeCl2.
分析 铁锈的主要成分是氧化铁,能和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的;
铁能和氯化铁反应生成氯化亚铁,氯化亚铁溶液是浅绿色的.
解答 解:(1)氧化铁和稀盐酸反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.
故填:Fe2O3+6HCl=2FeCl3+3H2O.
(2)课后清洗仪器时,一同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为氯化亚铁溶液.这是由于过量的铁继续与黄色溶液的主要成分反应造成的,该反应的化学方程式为:Fe+2FeCl3=3FeCl2.
故填:氯化亚铁;Fe+2FeCl3=3FeCl2.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
5.盐在日常生活中是用途非常广泛的一类物质.下列说法中不正确的是( )
| A. | 用食盐腌制食品,延长食品的保存期限 | |
| B. | 在蒸馒头时,用纯碱来消耗面团发酵生成的酸以调节口感 | |
| C. | 将草木灰(含K2CO3)与氯化铵混合施用来提高肥效 | |
| D. | 用石灰乳与硫酸铜溶液混合配制防治植物病害的农药 |
3.某合作学习小组讨论辨析以下说法:①纯净水和矿泉水都是纯净物;②金刚石和石墨都是由碳元素组成的单质;③煤、石油和天然气都是不可再生能源;④分子都比原子大;⑤CO和CO2都不能供给呼吸,都有毒性.其中正确的是( )
| A. | ②③ | B. | ①② | C. | ③④ | D. | ④⑤ |
10.下列物质属于纯净物的是( )
| A. | 冰水 | B. | 医用的生理盐水 | C. | 雪碧饮料 | D. | 稀有气体 |
7.甲、乙、丙三位同学决定探究盐酸溶液中到底是哪种粒子使紫色石蕊试液变红色.通过查阅资料得知其中只存在三种微粒为H2O、H+、Cl-.
(1)提出问题:是H2O、H+、Cl-中哪种粒子使紫色石蕊试液变红色?
(2)猜想:甲猜想:是H2O使紫色石蕊试液变红色
乙猜想:是H+使紫色石蕊试液变红色
丙猜想:使Cl-紫色石蕊试液变红色
(3)探究实验:
(4)结论与解释:根据上述实验现象及结论,可推断是H+粒子使紫色石蕊试液变红色.
(1)提出问题:是H2O、H+、Cl-中哪种粒子使紫色石蕊试液变红色?
(2)猜想:甲猜想:是H2O使紫色石蕊试液变红色
乙猜想:是H+使紫色石蕊试液变红色
丙猜想:使Cl-紫色石蕊试液变红色
(3)探究实验:
| 实验操作 | 现象 | 结论 |
| 1取少量蒸馏水滴加紫色石蕊试液. | 溶液不变色. | H2O不能(填“能”或“不能”)使紫色石蕊试液变红色. |
| 2另取少量氯化钠溶液于试管中,向其中滴加紫色石蕊试液. | 溶液不变色 | Cl-不能使紫色石蕊试液变红色. |
4.铁路列车实行大提速的有效措施是将原有铁路短轨或长轨焊接为超长轨,常用:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,这一反应原理来焊接钢轨.对该反应说法错误的是( )
| A. | 该反应是置换反应 | |
| B. | 根据反应,54g铝完全反应可以得到112g铁 | |
| C. | 反应前后元素的化合价都发生改变 | |
| D. | 在金属活动性顺序中:铝>铁 |
5.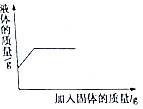 下列各项中的液体质量变化情况不能用如图所示的图象表示的是( )
下列各项中的液体质量变化情况不能用如图所示的图象表示的是( )
 下列各项中的液体质量变化情况不能用如图所示的图象表示的是( )
下列各项中的液体质量变化情况不能用如图所示的图象表示的是( )| A. | 把氯化钠加入一定量的蒸馏水中,配制生理盐水 | |
| B. | 把铁粉加入一定量的稀硫酸中制氢气 | |
| C. | 把碳酸氢钠固体加入一定量的稀盐酸中 | |
| D. | 将铝片放入一定量的硝酸镁溶液中 |