题目内容
1.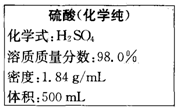 某校化学课外活动小组的同学需要一些稀硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图所示.请阅读标签上的说明,计算若需配制368.0g 19.6%的稀硫酸,应取该浓硫酸多少毫升.
某校化学课外活动小组的同学需要一些稀硫酸做化学实验.现有一瓶未开启的浓硫酸,标签如图所示.请阅读标签上的说明,计算若需配制368.0g 19.6%的稀硫酸,应取该浓硫酸多少毫升.
分析 根据溶质一定,利用溶质质量分数公式即可计算出应取该浓硫酸的质量,然后根据“体积=质量÷密度”即可计算出应取该浓硫酸的体积
解答 解:需要浓硫酸的质量为:368.0g×19.6%÷98.0%=73.6g,
浓硫酸的体积为:73.6g÷1.84g∕mL=40.0mL
答:应该取浓硫酸40mL.
点评 本题考查的是根据溶质质量分数的计算,完成此题,可以依据已有的公式进行,抓住稀释前后溶质的质量不变.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
12.测知CO和M的混合体气体中,氧的质量分数为40%,则M气体可能是( )
| A. | CO2 | B. | N2O | C. | SO2 | D. | SO3 |
9.地壳中含量(质量分数)最多的非金属元素和金属元素形成的化合物是( )
| A. | AlO | B. | OAl | C. | Al3O2 | D. | Al2O3 |
16.下列物质的转化中只有加入酸才能一步实现的是( )
| A. | Zn→ZnSO4 | B. | CaCO3→CO2 | C. | MgO→MgCl2 | D. | BaCl2→BaSO4 |