题目内容
14.如图所示为实验室中常见的气体制备和收集装置.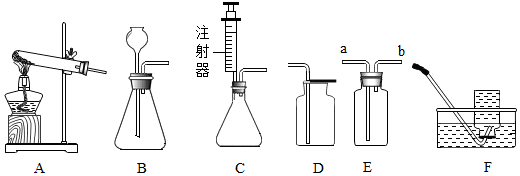
请回答下列问题:
(1)实验室用双氧水溶液和二氧化锰制取氧气,反应的化学表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,二氧化锰起催化作用.
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是控制反应物的量,从而控制化学反应的速率.
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从a(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b(填“a”或“b”)端通入.
(4)汽车尾气中的一氧化氮是一种大气污染物.它是一种无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体.实验室中制取一氧化氮采用的收集装置是F(填序号).
(5)选择气体的发生装置时,应该考虑的因素有:反应物的状态和反应条件.甲烷是最简单的有机物类的气体,实验室常用加热醋酸钠与氢氧化钠固体混合物来制得.实验室制取甲烷应选用的发生装置是(填序号)A.
分析 (1)二氧化锰在过氧化氢分解中起催化作用,依据反应原理书写方程式;
(2)观察图形可知,C是用注射器添加液体,然后考虑注射器的优点进行分析解答.
(3)欲使用装置E用排空气法收集氧气,因为氧气的密度比空气的密度大,所以气体应从a进入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b进入,因为气体的密度比水的密度小;
(4)因为一氧化氮气体难溶于水,在空气中容易与氧气发生反应,因此一氧化氮只能用排水法收集;
(5)根据实验室常用加热醋酸钠与氢氧化钠固体混合物来制得属于固固加热型解答.
解答 解:(1)用双氧水和二氧化锰来制取氧气时,其中二氧化锰起催化作用.该反应的化学符号表达式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)装置C滴加液体的仪器是注射器,用注射器代替长颈漏斗,可以使滴加的液体随加随停,可控制产生气体的速率.
(3)欲使用装置E用排空气法收集二氧化碳,因为二氧化碳的密度比空气的密度大,因此应该从a进入.欲使用装置E用排水法收集氧气,先将瓶中装满水,因为气体的密度总比水的密度小,因此再将气体从b进入即可,
(4)因为一氧化氮气体难溶于水,在空气中容易与氧气发生反应,因此一氧化氮只能用排水法收集,答案为:F;
(5)选择气体的发生装置时,应该考虑的因素有:反应物的状态和反应条件;实验室常用加热醋酸钠与氢氧化钠固体混合物来制得.实验室制取甲烷应选用的发生装置是A.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,催化;
(2)控制反应物的量,从而控制化学反应的速率;
(3)a;b;
(4)F;
(5)反应物的状态和反应条件;A.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

| A. | 该物质由碳、氢、氧三种元素组成 | |
| B. | 该物质中碳、氢、氧元素的质量比是9:1:2 | |
| C. | 该物质的分子中原子个数比依次为3:4:1 | |
| D. | 该物质的相对分子质量为56 |
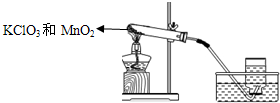 兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见表:
兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见表:| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(2)完全反应后剩余固体中含有什么物质?质量各多少克?(请写出规范的解题过程)
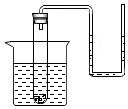 把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )
把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )| A. | 减少、左高右低 | B. | 增加、左高右低 | C. | 减少、左低右高 | D. | 增加、左低右高 |
| A. | SiO2 | B. | Fe20 | C. | Al03 | D. | Al2 03 |
| A. | NH4+、Cu2+、SO42-、NO3- | B. | K+、Ba2+、Cl-、SO32- | ||
| C. | K+、MnO4-、NH4+、CH2COO- | D. | Na+、K+、HCO3-、NO3- |